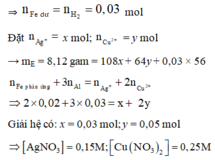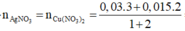Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A.
Vì phản ứng giữa Al và AgNO3 xảy ra trước nên kim loại sau phản ứng phải có Ag, kế đến là CuSO4 có phản ứng tạo thành Cu. Theo giả thiết, có ba kim loại → kim loại thứ ba là Fe còn dư.
Ta có: nFe = 2,8/5,6 = 0,05 (mol)
nAl = 0,81/27 = 0,03 (mol)
và = 0,672/22,4 = 0,03 (mol)
Phản ứng: Fedư + 2HCl → FeCl2 + H2
(mol) 0,03 0,03
→ Số mol Fe phản ứng với muối: 0,05 – 0,03 = 0,02 (mol)
2Al + 3Cu2+ → 2Al3+ + 3Cu
Fe + 2Ag+ → Fe2+ + 2Ag
Fe + Cu2+ → Fe2+ + Cu
Ta có sự trao đổi electron như sau:
Al → Al3+ + 3e Fe → Fe2+ + 2e
0,03 0,09 (mol) 0,02 0,04 (mol)
Ag+ + 1e → Ag Cu2+ + 2e → Cu
x x x (mol) y 2y y (mol)
→ x + 2y = 0,09 + 0,04 = 0,13 (1) ; 108x + 64y + 56.0,03 = 8,12 (2)
Giải hệ phương trình (1) và (2), ta được x = 0,03; y = 0,05.
Vậy:


Đáp án A
Vì T chứa 3 kim loại nên T chứa Cu, Ag và Fe dư (Al phản ứng trước Fe).
Khi đó Al, Cu2+ và Ag+ phản ứng hết.
Khi cho T phản ứng với HCl dư, chỉ có Fe phản ứng
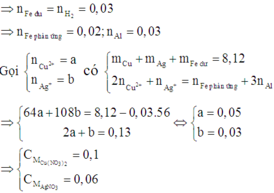

Cho Y chứa 3 kim loại, tác dụng với dung dịch HCl dư thu được 0,035 mol khí H2 → Y chứa Fe dư
Vậy Y chứa Cu : x mol , Ag: x mol và Fe dư : 0,035 mol
⇒ Fe pư : 0,05 - 0,035 = 0,015 mol
Bảo toàn electron → 2nCu(NO3)2 + nAgNO3 = 2nFe + 3nAl
⇒ 2x + x = 2. 0,015 + 0,03. 3 → x = 0,04 mol
⇒ CMCu(NO3)2 = CMAgNO3 = 0,04 : 0,1 = 0,4M
Đáp án B

Đáp án D
Vì dung dịch C đã mất màu hoàn toàn nên cả Ag+ và Cu2+ đều phản ứng hết.
Mà B không tan trong HCl nên B chỉ chứa Ag và Cu. Do đó cả Al và Fe đều phản ứng hết.
Suy ra cho X vào A thì cả 4 chất đều phản ứng vừa đủ.
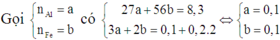
Vì dung dịch E đã nhạt màu nên Ag+ đã phản ứng hết và Cu2+ đã phản ứng một phần.
Do đó D chứa Ag và Cu.
Dung dịch E chứa Al3+, Fe2+ và Cu2+ dư. Khi đó E chứa Fe(OH)2 và Cu(OH)2
Suy ra F chứa Fe2O3 và CuO
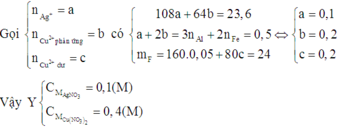

Fedư => AgNO3,Cu(NO3)2 và Al phản ứng hết, phản ứng
Bảo toàn electron ta có: ne cho= nenhận
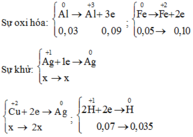
Bảo toàn electron ta có: ne cho= nenhận
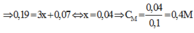

Đáp án D
Cho hỗn hợp kim loại trên vào dung dịch chứa FeCl3 và CuCl2 sau phản ứng thu được dung dịch X và rắn Y. Cho AgNO3 dư vào X thấy AgNO3 phản ứng 0,54 mol và thu được kết tủa là AgCl và Ag.
Giải được số mol AgCl và Ag lần lượt là 0,48 và 0,06 mol.
Gọi số mol FeCl3 lần lượt là a thì số mol CuCl2 là 1,5a
Bảo toàn Cl: 3 a + 1 , 5 a . 2 = 0 , 48 → a = 0 , 08 m o l
Ta có số mol Ag là 0,06 nên số mol FeCl2 trong X phải là 0,06 mol.
Do vậy chỉ có Al phản ứng với dung dịch muối ban đầu vì số mol FeCl2 nhỏ hơn FeCl3.
→ n A l = 0 , 08 + 0 , 02 . 2 + 0 , 12 . 2 3 = 0 , 12 = n F e
Do vậy rắn Y chứa Fe 0,14 mol, Cu 0,12 mol
→ x = 15 , 52 g a m

Chọn A.
Hỗn hợp X gồm Mg (4x mol) và Fe (3x mol) và dung dịch chứa FeCl3 (6y mol) và CuCl2 (y mol)
Dung dịch Y chứa Fe2+, Mg2+ (4x mol) và Cl- (20y mol)