Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Muối sau pư gồm \(\left\{{}\begin{matrix}Fe\left(NO_3\right)_3:1\left(mol\right)\\Zn\left(NO_3\right)_2:0,6\left(mol\right)\end{matrix}\right.\)
Bảo toàn N: nHNO3 = 5,4 (mol)

Ở ví dụ 4, ta đã giải quyết câu hỏi này bằng bảo toàn nguyên tố, giờ với phương trình liên hệ mol H+ và sản phẩm khử, ta có ngay: nH+ = 12nN2 + 4nNO = 12.0,01 + 4.0,02 =0,2 mol
Chọn đáp án D

Ta có: \(n_{NO}+n_{N_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\left(1\right)\)
\(30n_{NO}+28n_{N_2}=1,44\left(g\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,02\left(mol\right)\\n_{N_2}=0,03\left(mol\right)\end{matrix}\right.\)
Gọi nNH4NO3 = a (mol)
⇒ nNO3- (trong muối) = 3nNO + 10nN2 + 8nNH4NO3 = 0,36 + 8a (mol)
Ta có: m muối = mKL + mNO3- (trong muối) + mNH4NO3
⇒ 66,88 = 10 + 62.(0,36 + 8a) + 80a
⇒ a = 0,06 (mol)
⇒ nHNO3 = 4nNO + 12nN2 + 10nNH4NO3 = 1,04 (mol)

Fe, Cu + O2 → hỗn hợp rắn X
Theo ĐL Bảo toàn khối lượng có mO2= 63,2-56a-0,15.64= 53,6-56a (gam) → nO2= (53,6-56a)/32 mol
Ta có nNO= 0,2 mol
QT cho e:
Fe→ Fe3++ 3e
a 3amol
Cu → Cu2++ 2e
0,15 0,3
QT nhận e :
O2+ 4e→ 2O-2
(53,6-56a)/32 (53,6-56a)/8
N+5+ 3e → NO
0,6←0,2
Theo ĐL BT electron thì : ne cho= ne nhận
Nên 3a+ 0,3= (53,6-56a)/8+ 0,6 Suy ra a= 0,7
Đáp án C

Khối lượng Fe dư là 1,46g, do đó khối lượng Fe và Fe3O4 đã phản ứng là 17,04g. Vì sau phản ứng sắt còn dư nên trong dung dịch D chỉ chứa muối sắt (II).
Sơ đồ phản ứng:
Fe, Fe3O4 + HNO3 → Fe(NO3)2 + NO + H2O
Mol: 2n+0,1 n 0,1 0,5( 2n+0,1)
Đặt số mol của Fe(NO3)2 là n, áp dụng định luật bảo toàn nguyên tố đối với nitơ ta có số mol của axit HNO3 là 2n+ 0,1. Số mol H2O bằng một nửa số mol của HNO3.
Áp dụng định luật bảo toàn khối lượng ta có:
17,04 + 63(2n + 0,1) = 242n + 0,1.30 + 18.0,5(2n + 0,1)
giải ra ta có n = 2,7, suy ra [ HNO3 ] = (2.2,7 + 0,1): 0,2 = 3,2M
Đáp án A





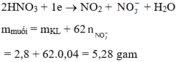
Sau phản ứng, Fe dư. $n_{Fe\ dư} = \dfrac{2,8}{56} = 0,05(mol)$
$\Rightarrow n_{Fe\ pư} = 0,35 - 0,05 = 0,3(mol)$
Bảo toàn electron :
$3n_{Al} + 2n_{Fe\ pư} = 8n_{NH_4NO_3} + 8n_{N_2O} + 10n_{N_2}$
$\Rightarrow n_{NH_4NO_3} = 0,05(mol)$
$n_{Fe(NO_3)_2} = n_{Fe\ pư} = 0,3(mol)$
$n_{Al(NO_3)_3} = n_{Al} = 0,2(mol)$
Ta có, Bảo toàn nguyên tố N :
$n_{HNO_3} = 2n_{Fe(NO_3)_2} + 3n_{Al(NO_3)_3} + 2n_{NH_4NO_3} + 2n_{N_2O} + 2n_{N_2} = 1,48(mol)$
$V = \dfrac{1,48}{1} = 1,48(lít)$