Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

X: Fe3O4
Y: FeCl2
Z: FeCl3
T: Fe(OH)2
U: Fe(OH)3
A: NaCl (hoặc H2O)
B: H2O (hoặc NaCl)
D: H2 (hoặc Cl2)
E: Cl2 (hoặc H2)
F: NaOH
G: HCl
PTHH:
a) NaCl + H2O -dpmn----> 1/2 H2 + 1/2 Cl2 + NaOH
H2 + Cl2 -to-> 2 HCl
HCl + NaOH -> NaCl + H2O
b) 3 Fe +2 O2 -to->Fe3O4
Fe3O4 + 8 HCl -> FeCl2 +2 FeCl3 + H2O
FeCl2 + 2 NaOH -> Fe(OH)2 + 2 NaCl
FeCl3 +3 NaOH -> Fe(OH)3 + 3NaCl
Chúc em học tốt!

a) ch4+202=>co2+2h2o (đk nhiệt độ) (1)
b) theo bài ra :
nCH4=4,48/22,4=0,2 mol
theo (1): nO2=2 nCH4=2*0,2=0,4 mol
=> VO2=0,4*22,4=8,96 lít
theo (1): n CO2=nCH4=0,2 mol
=> V CO2=0,2*22,4=4,48 lít
a. \(CH_4+2O_2->CO_2+2H_2O\)
b. 22,4l khí mê tan cần dùng 44,8l khí Oxi và tạo ra 22,4l khí cacbon đioxit
Vậy 4,48l mê tan cần dùng 8,96l khí Oxi và tạo ra 4,48l khí cacbon đioxit

Phản ứng oxi hóa khử giữa oxit kim loại và CO cần điều kiện ở nhiệt độ cao nhé
Nhưng mà nó có hai trường hợp xảy ra.
Khi nào phản ứng này xảy ra zậy a: Fe203+Co--->fe304+ Co2 zay a

\(CH_3COOH+C_2H_5OH< =\left(H_2SO_4đ,t^o\right)=>CH_3COOC_2H_5+H_2O\)
\(n_{CH_3COOH}=\dfrac{60}{60}=1\left(mol\right)\)
Theo PTHH: \(n_{CH_3COOC_2H_5}\left(lt\right)=1\left(mol\right)\)
Vì \(H=90\%\)
\(\Rightarrow n_{CH_3COOC_2H_5}\left(tt\right)=\dfrac{1.90}{100}=0,9\left(mol\right)\)
Khối lượng Elyl Axetat thu được là:
\(\Rightarrow m_{CH_3COOC_2H_5}\left(tt\right)=0,9.88=79,2\left(g\right)\)

$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(1)$
$Fe_2(SO_4)_3 + Fe\ to 3FeSO_4(2)$
Gọi $n_{Fe_2(SO_4)_3} = a(mol) ; n_{FeSO_4} = b(mol)$
Ta có : $400a + 152b = 62,8(1)$
$n_{SO_2} = 0,15(mol)$
$n_{Fe_2(SO_4)_3(1)} = \dfrac{1}{3}n_{SO_2} = 0,05(mol)$
$n_{Fe_2(SO_4)_3(2)} = \dfrac{1}{3}n_{FeSO_4} = \dfrac{b}{3}$
Suy ra:
$0,05 - \dfrac{b}{3} = a(2)$
Từ (1)(2) suy ra $a = \dfrac{45}{112} ; b = -1,055<0$
=> Sai đề

\(n_{CaCO_3}=\dfrac{m}{M}=\dfrac{7}{100}=0.07\left(mol\right)\);
\(n_{H_2SO_4}=C_M.V=0,2.0,5=0,1\)(mol)
PTHH : CaCO3 + H2SO4 ---> CaSO4 + H2O + CO2
1 : 1 : 1 : 1 : 1
Dễ thấy : \(\dfrac{n_{CaCO_3}}{1}< \dfrac{n_{H_2SO_4}}{1}\)
=> H2SO4 dư ; tính chất theo \(n_{CaCO_3}\)
=> \(n_{CO_2}=0,07\left(mol\right)\)
=> \(V_{CO_2\left(đktc\right)}=n.22,4=0,07.22,4=1,568\left(l\right)\)
\(V_{CO_2\left(đkt\right)}=C_M.V=0,07.24=1,68\left(l\right)\)

SO3 + H2O ---> H2SO4
H2SO4 + 2NaOH ---> Na2SO4 + H2O
SO2 + 2NaOH ---> Na2SO3 + H2O
SO2 + NaOH ---> NaHSO3
Nếu x >= 2b tạo ra muối Na2SO3
Nếu x <= b tạo ra muối NaHSO3
Nếu b < x < 2b tạo ra cả 2 muối NaHSO3 và Na2SO3.
Với mọi a và x luôn tạo ra muối Na2SO4.

Đặt CTHH của oxit sắt cần tìm : FexOy
PTHH : FexOy + yH2 = xFe + yH2O
0.2
Theo giả thiết C%H2SO4 còn 98% -3.405%= 94.595%
Hoặc \(\dfrac{98}{100+m_{H2O}}\) =0.94595
giải được mH2O=3.6g
nH2O=0.2 mol
Chất rắn thu được là Fe , nH2 thoát ra=3.36/22.4=0.15 mol
PTHH : Fe + H2SO4 --> FeSO4 + H2
0.15 0.15
Ta có tỉ lệ : nFe:nH2O = x:y = 0,15:0,2 = 3:4
Vậy CTHH của oxit sắt là Fe3O4


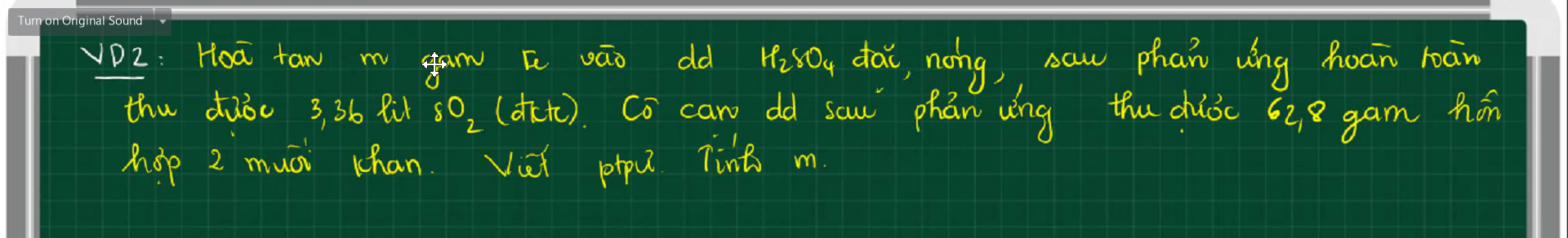

Với:
\(\)\(n_{SO_2}=n_{Ba\left(OH\right)_2}\)hoặc \(n_{SO_2}< n_{Ba\left(OH\right)_2}\) sinh ra \(BaSO_3\)
Với :
\(n_{Ba\left(OH\right)_2}=2n_{SO_2}\) hoặc \(n_{Ba\left(OH\right)_2}< 2n_{SO_2}\) sinh ra \(Ba\left(HSO_3\right)_2\)