Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Xét phần 2: nBaSO4 = 0,24 mol ⇒ y = 0,24 ÷ 3 = 0,08 mol.
Xét phần 1: nOH– = 0,9 mol > 3nAl(OH)3 = 3 × 0,22
⇒ nOH– = 4nAl3+ - n↓ ⇒ nAl3+ = (0,22 + 0,9)/4 = 0,28 mol.
⇒ x = 0,28 - 0,08 × 2 = 0,12 ⇒ x : y = 3 : 2 ⇒ chọn A.

Chọn D
nAl2(SO4)3 = 0,01 ⇒ nAl3+ = 0,02 mà nAl(OH)3 = 0,01 < 0,02 nên có 2 trường hợp
Trường hợp 1: nOH-min = 3nAl(OH)3 = 0,03 ⇒ [NaOH] = 0,03/0,025 = 1,2M.
Trường hợp 2: nOH-max = 4nAl3+ – nAl(OH)3 = 4.0,02 – 0,01 = 0,07
⇒ [NaOH] = 0,07/0,025 = 2,8M

Chỉ có Al3+ phản ứng với OH- tạo kết tủa Al(OH)3, còn Na+ không p.ư với OH-
nAl3+ = 0,04 mol; nSO42- = 0,08 mol; nOH- = 0,14 mol; nBa2+ = 0,07 mol.
nBaSO4 = 0,07 mol;
Al3+ + 3OH- ---> Al(OH)3
0,04 0,12 0,04
Al(OH)3 + OH- ---> AlO2- + 2H2O
0,04 0,02
nAl(OH)3 = 0,02 mol.
Vậy kết tủa gồm Al(OH)3 và BaSO4 có tổng khối lượng = 78.0,02 + 233.0,07 = 17,87 gam.

Đáp án A
Sinh khí H2 ⇒ dung dịch X không chứa NO3–. Al là kim loại mạnh ⇒ chú ý có NH4+!
► Ta có sơ đồ phản ứng sau:
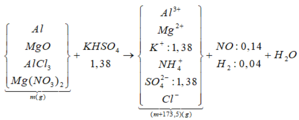
A. 6,912.

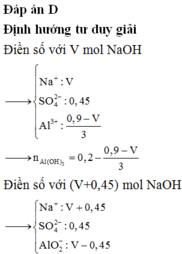
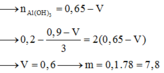
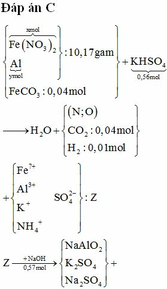


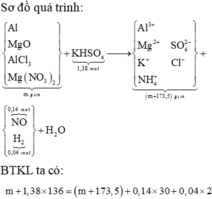


Đáp án D