Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{AgNO_3}=0,5.0,2=0,1\left(mol\right)\)
Gọi công thức chung của 2 muối là NaT
PTHH: NaT + AgNO3 --> NaNO3 + AgT
0,1---------------->0,1
=> \(M_{AgT}=\dfrac{16,8}{0,1}=168\left(g/mol\right)\)
=> MT = 60(g/mol)
Mà 2 halogen liên tiếp nhau
=> X là Cl(Clo), Y là Br(Brom)

Đáp án C
Gọi công thức chung của NaX và NaY là NaM.
NaM + AgNO3 → AgM↓+NaNO3
0,03 →0,03 (mol)
![]()
=> M = 50,3 => X,Y lần lượt là Cl và Br

Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)

Quy NaX và NaY về NaR
\(n_{AgNO_3}=0,15.0,2=0,05\left(mol\right)\)
PTHH: \(AgNO_3+NaR\rightarrow AgR\downarrow+NaNO_3\)
0,05------>0,05
\(\rightarrow M_R=\dfrac{2,2}{0,05}=44\left(g\text{/}mol\right)\)
Mà X và Y là 2 nguyên tố halogen thuộc 2 chu kì liên tiếp
\(\rightarrow M_X< M_R< M_Y\rightarrow M_X< 44< M_Y\)
---> X và Y là Cl và Br

1.
TH1: Không có muối của Flo \(\Rightarrow\) Tạo 2 kết tủa
\(NaB+AgNO_3\rightarrow NaNO_3+AgB\)
0,03______0,03______0,03__________
\(n_{AgNO_3}=0,15.0,2=0,03\left(mol\right)\)
\(\Rightarrow m_{NaB}=0,03.\left(23+M_B\right)=2,2\)
\(\Rightarrow M_B=50,33\)
\(\Rightarrow M_X< 50,33< M_Y\)
Vì X, Y thuộc 2 chu kỳ liên tiếp nên X, Y lần lượt là: Cl và Br
\(m_{NaNO3}=0,03.85=2,55\left(g\right)\)
Theo ĐLBTKL, ta có:
mAgB = ( mNaB + mAgNO3 ) - mNaNO3
\(=\left(2,2+5,1\right)-2,55=4,75\left(g\right)\)
TH2: Có muối của flo \(\Rightarrow\) Có 1 kết tủa là AgCl
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\)
\(n_{AgCl}=n_{AgNO3}=0,03\left(mol\right)\)
\(\Rightarrow m_{AgCl}=0,03.143,5=4,305\left(g\right)\)

TH1: NaF và NaCl
Kết tủa chỉ có AgCl
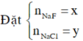
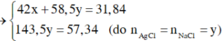
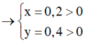
Vậy CT 2 muối có thể là NaF và NaCl
TH2: Hỗn hợp muối không chứa NaF
Đặt CT chung của 2 muối ban đầu là NaX
![]()
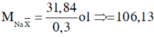
=> 2 muối là NaBr và NaI
Đáp án A

Bài 1 ⅕ dd A có mH2O=92,7/5=18,54g
HCl + AgNO3 =>AgCl + HNO3
0,04 mol<=0,04 mol<=0,04 mol
nAgCl=5,74/143,5=0,04 mol
mHCl=0,04.36,5=1,46g
mddHCl=0,04.36,5+18,54=20g
C%dd HCl=C%dd A=1,46/20.100%=7,3%
Bài 2
TH1 2 Halogen là F và Cl
n ktủa=nAgCl=4,75/143,5=0,033 mol>0,03 mol hh 2 muối
=>loại
TH2 2 Halogen không phải F và Cl
Gọi Hal trung bình là Z
nAgZ=4,75/(108+Z) mol
nhh muối=0,03 mol
NaZ + AgNO3 =>AgZ + NaNO3
0,03 mol =>0,03 mol
=>4,75/0,03=108+Z=>Z=50,33g/mol
Mà 2 halogen ở 2 chu kì kế tiếp nhau
=>2 halogen là Cl và Br


Trường hợp 1 : Nếu chỉ có 1 chất kết tủa.
Suy ra : hai muối gồm : $NaF(a\ mol) ; NaCl(b\ mol)$
$NaCl + AgNO_3 \to AgCl + NaNO_3$
Ta có :
$m_{hh} = 42a + 58,5b = 35,6(gam)$
$m_{AgCl} = 143,5b = 61,1(gam)$
Suy ra: a = 0,25456 ; b = 0,42578
$\%m_{NaF} = \dfrac{0,25456.42}{35,6}.100\% = 30,03\%$
$\%M_{NaCl} = 100\% - 30,03\% = 69,97\%$
Trường hợp 2 : Nếu có 2 chất kết tủa
Gọi công thức tổng quát của 2 muối là $NaR$
$NaR + AgNO_3 \to AgR + NaNO_3$
Theo PTHH :
$n_{NaR} = n_{AgR} \Rightarrow \dfrac{35,6}{23 + R} = \dfrac{61,1}{108+R}$
$\Rightarrow R = 95,67$
Ta thấy : $M_{Br} < R <M_I$ nên V gồm $NaBr(x\ mol) ; NaI(y\ mol)$
Ta có :
$m_V = 103x + 150y = 35,6(gam)$
$m_{kết\ tủa} = 188x + 235y = 61,1(gam)$
Suy ra: x = 0,2 ; y = 0,1
$\%m_{NaBr} = \dfrac{0,2.103}{35,6}.100\% = 57,87\%$
$\%m_{NaI} = 100\% - 57,87\% = 42,13\%$