Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Fe + S → FeS(1)
FeS + H2SO4 → FeSO4 + H2S (2)
Fe + H2SO4 → FeSO4 + H2 (3)
H2 + S → H2S (4)
Vai trò của S trong phản ứng (1), (4) : S là chất oxi hóa.

a)
$2K + 2H_2O \to 2KOH + H_2$
$K_2O + H_2O \to 2KOH$
$SO_2 + H_2O \to H_2SO_3$
$P_2O_5 + 3H_2O \to 2H_3PO_4$
b)
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$Cu + Cl_2 \xrightarrow{t^o} CuCl_2$
$2K + Cl_2 \xrightarrow{t^o} 2KCl$
$2KOH + Cl_2 \to KCl + KClO + H_2O$
c)
$F e+ 2HCl \to FeCl_2 + H_2$
$2K + 2HCl \to 2KCl + H_2$
$CuO + 2HCl \to CuCl_2 + H_2O$
$K_2O + 2HCl \to 2KCl + H_2O$
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
$KOH + HCl \to KCl + H_2O$
$Zn(OH)_2 + 2HCl \to ZnCl_2 + H_2O$
$AgNO_3 + HCl \to AgCl + HNO_3$
$CaCO_3 + 2HCl \to CaCl_2 + CO_2 + H_2O$
d)
$Fe + CuCl_2 \to FeCl_2 + Cu$
$2KOH + CuCl_2 \to Cu(OH)_2 + 2KCl$
$2AgNO_3 + CuCl_2 \to 2AgCl + Cu(NO_3)_2$

\(a)\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\)
\(b)\ n_{H_2} = \dfrac{1,12}{22,4} = 0,05(mol)\\ n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{0,1}{3}(mol)\\ \Rightarrow m_{Al} = \dfrac{0,1}{3}.27= 0,9\ gam\)
\(c)\ n_{HCl} = 2n_{H_2} = 0,05.2 = 0,1(mol)\\ \Rightarrow C_{M_{HCl}} = \dfrac{0,1}{0,2} = 0,5M\)
a) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b) Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(\Rightarrow n_{Al}=\dfrac{1}{30}\left(mol\right)\) \(\Rightarrow m_{Al}=\dfrac{1}{30}\cdot27=0,9\left(g\right)\)
b) Theo PTHH: \(n_{HCl}=2n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)

\(Cu+H_2SO_{4\left(loãng\right)}-\times\rightarrow\\ 2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ K_2S+H_2SO_4\rightarrow K_2SO_4+H_2S\uparrow\\ MgCl_2+H_2SO_4-\times\rightarrow\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
---> có 3 phản ứng

Bài 1)
Mg(OH)2 + H2SO4 => MgSO4 + 2H20
Bài 2)
sinh ra dd ko màu thì chỉ có Al2O3 thôi
Bài 3)
MgO + 2HNO3 => Mg(NO3)2 + H2O
Bài 4)
phương pháp hóa học
+ lấy hh Fe, Cu tác dụng với HCl
Fe +2 HCl => FeCl2 + H2
+ còn đồng ko tác dụng dc với HCl : ta lọc đồng ra khỏi hh òi phơi khô. Ta giả định cho đồng là 4g => mFe = 6g
% Cu = 4*100/10 = 40(%)
% Fe = 100- 40= 60 (%)
phương pháp vật lý
dùng nam châm hút sắt ra khỏi hỗn hợp. Ta có mFe là 6g => m Cu = 4 (g)
% Cu = 4*100/10 = 40(%)
% Fe = 100-40 = 60(%)

Câu 1 :
a) $Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O$
b) SO2 là khí không màu ,mùi sốc,nặng hơn không khí, tan nhiều trong nước.
c) n Cu = n SO2 = 6,72/22,4 = 0,3(mol)
m Cu = 0,3.64 = 19,2(gam)
m Fe = 28,9 - 19,2 = 9,7(gam)
d)
%m Cu = 19,2/28,9 .100% = 66,44%
%m Fe = 100% -66,44% = 33,56%
Câu 2 :
a) $Zn + 2H_2SO_4 \to ZnSO_4 + SO_2 + H_2O$
b) SO2 là khí không màu ,mùi sốc,nặng hơn không khí, tan nhiều trong nước
c) n Zn = n SO2 = 8,96/22,4 = 0,4(mol)
m Zn = 0,4.65 = 26(gam)
m Al = 30,5 -26 = 4,5(gam)
d)
%m Zn = 26/30,5 .100% = 85,25%
%m Al = 100%- 85,25% = 14,75%
Câu 3 :
Tác dụng với H2SO4 loãng : Fe,CuO,FeS
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
$FeS + H_2SO_4 \to FeSO_4 + H_2S$
Tác dụng với H2SO4 đặc : Fe,Cu,CuO,FeS
$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
$Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O$
$2FeS + 10H_2SO_4 \to Fe_2(SO_4)_3 + 9SO_2 + 10H_2O$

Câu 1:
a) \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(\dfrac{1}{2}Cl_2+K\underrightarrow{t^o}KCl\)
\(2KCl+2H_2O\xrightarrow[cómàngngăn]{đp}2KOH+Cl_2+H_2\)
\(Cl_2+H_2O⇌HCl+HClO\)
\(NaOH+HClO\rightarrow NaClO+H_2O\)
\(NaClO_{\left(rắn\right)}+HCl\rightarrow NaCl+Cl_2+H_2O\)
\(2NaCl+2H_2O\xrightarrow[cómàngngăn]{đp}2NaOH+Cl_2+H_2O\)
\(3Cl_2+2Fe\underrightarrow{t^o}2FeCl_3\)
b) \(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(Cl_2+H_2\underrightarrow{a/s}2HCl\)
\(2HCl+Fe\rightarrow FeCl_2+H_2\)
\(2FeCl_2+Cl_2\rightarrow2FeCl_3\)
\(FeCl_3+3KOH\rightarrow3KCl+Fe\left(OH\right)_3\downarrow\)
\(2KCl+2H_2O\xrightarrow[cmn]{đp}2KOH+Cl_2+H_2\)
\(6KOH+3Cl_2\underrightarrow{t^o}5KCl+KClO_3+3H_2O\)
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)

Với dung dịch H2SO4 loãng :
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Fe3O4 + 4H2SO4 → Fe2(SO4)3 + FeSO4 + 4H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Với dung dịch KOH
2Al + 2KOH + 2H2O → 2KAIO2 + H2O
Al2O3 + 2KOH → 2KAIO2 + H2O

Phương trình hóa học của phản ứng:
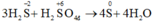
Do H2S có tính khử và H2SO4 có tính oxi hóa nên chúng có khả năng tác dụng với nhau sinh ra kết tủa vàng là S
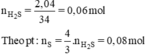
mS = 0,08 × 32 = 2,56g.
Phản ứng HCl: KOH,CaO,Mg
Ptpu: KOH + HCl -> KCl + H2O
CaO + 2HCl -> CaCl2 + H2O
Mg + 2HCl -> MgCl2 + H2
Phản ứng H2SO4: KOH, CaO, Mg
2KOH + H2SO4 -> K2SO4 +H2O
CaO + H2SO4 -> CaSO4 + H2O
Mg + H2SO4 -> MgSO4 + H2