Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B:
![]()
có 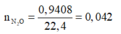
Gọi n là hóa trị của kim loại M. Các quá trình nhuờng và nhận electron:
Quá trình nhường electron: ![]()
Quá trình nhận electron: ![]()
Áp dụng định luật bảo toàn mol electron, ta có: ![]()
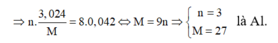

Đáp án B
MKhí = 22 chứng tỏ NxOy là N2O duy nhất
nN2O = 0,042 mol
2N+5+ 8e → N2O M→Mn++ne
0,336 0,042
BT e ⇒ne = 0,036 mol⇒nM = 0,036 /n
Khi đó M=3,024/ (0,336:n)
M=9n ⇒ n=3, M=27⇒ Chọn Al

Đặt nMg = a
nAl = b
Ta có, hệ pt: 24a + 27b = 9
2a + 3b = 0.3x3
=> a = 0.15, b= 0.2
%mMg = 40%
%mAl = 60%
Khi cho KOH dư thì Al(OH)3 sẽ tan tạo KAlO2 => m tủa = m Mg(OH)2 = 0.15x58 = 8,7 (g)

Đáp án B
- Khi cho hỗn hợp tác dụng với H2SO4 loãng dư chỉ có Mg phản ứng sinh ra khí H2 => nMg=nH2=0,15 mol
- Khi cho hỗn hợp tác dụng với HNO3 dư => Chỉ có Cu và Mg (kim loại thay đổi số oxi hóa)
BT e: nCu=(3nNO-2nMg)/2=0,15 mol
=>mCu=0,15.64=9,6 gam

Đặt số mol NO và N2O trong 8,96 l hỗn hợp A lần lượt là x và y.
Ta có:
Từ (I, II): x = 0,3 và y = 0,1
Các phương trình phản ứng:
Al + 4HNO3 → Al(NO3)3 + NO↑ + 2H2O (1)
0,03mol ← 0,3 mol
8 Al + 30HNO3 → 8Al(NO3)3 + 3N2O↑ + 15H2O (2)
← 0,1 mol
xin lỗi nha nhưng tui ko hiểu. Bạn viết chi tiết gium nha. Chỉ có 1 chất khử thôi mà