Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do hiệu suất phản ứng là 25% nên
VN2 pứ= 4.25%= 1 lít; VH2 pứ= 12.25%= 3 lít;
VNH3 sinh ra= 2VN2 pứ= 2 lít
VN2 dư= 4-1=3 lít, VH2 dư= 12-3=9 lít
Hỗn hợp thu được sau phản ứng có thể tích là
V= VN2 dư+ VH2 dư+ VNH3 sinh ra= 3 +9+2=14 lít
Đáp án B

Đáp án A.
N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do 4 1 < 14 3 →Hiệu suất tính theo N2
Đặt thể tích N2 phản ứng là x lít
→VH2 pứ= 3x lít, VNH3 sinh ra=2xlít
VN2 dư= 4-x (lít), VH2 dư= 14-3x (lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được là
V khí= VH2 dư+ VN2 dư+ VNH3= 14-3x + 4-x+ 2x= 16,4
→ x=0,8 lít
→ H = v N 2 pu V N 2 bd · 100 % = 0 , 8 4 · 100 % = 20 %

Chọn đáp án C
Ta có phản ứng
1N2 + 3H2 ⇌ 2NH3
Hiệu suất tính theo N2 vì:  .
.
nN2 pứ = ![]()
⇒ Hpứ =![]()

Đáp án B.
N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do 25 1 > 60 3 →Hiệu suất tính theo H2
Đặt thể tích H2 phản ứng là x lít
→VN2 pứ= x/3 lít, VNH3 sinh ra=2x/3 lít
VN2 dư= 25-x/3 (lít), VH2 dư= 60- x(lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được là
V khí= VH2 dư+ VN2 dư+ VNH3= 60-x+ 25-x/3+ 2x/3= 75
→ x=15 lít

Đáp án : C
Ta có Cùng điều kiện -> Quy số lít về số mol.n(hh ban đầu) = 20 mol; n(hh sau) = 16 lít
=> H2 phản ứng mất 4 lít => C2H2 có 2 lít và CH4 có 8 lít
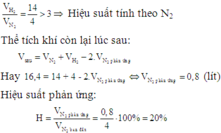
Gọi \(n_{N_2}=a\left(mol\right)\)
PTHH: \(N_2+3H_2\xrightarrow[]{t^o,p,xt}2NH_3\)
a--->3a---------->2a
=> Hỗn hợp sau phản ứng có \(\left\{{}\begin{matrix}n_{N_2}=9-a\left(mol\right)\\n_{H_2}=6-3a\left(mol\right)\\n_{NH_3}=2a\left(mol\right)\end{matrix}\right.\)
a) Vì hh sau phản ứng có 14 lít khí
=> 9 - a + 6 - 3a + 2a = 14
=> a = 0,5 (lít)
=> \(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{9-0,5}{14}.100\%=60,71\%\\\%V_{H_2}=\dfrac{6-0,5.3}{14}.100\%=32,14\%\\\%V_{NH_3}=\left(100-60,71-32,14\right)\%=7,15\%\end{matrix}\right.\)
b) Vì NH3 chiếm 20% thể tích hỗn hợp
=> \(\dfrac{2a}{9-a+6-3a+2a}.100\%=20\%\)
=> \(a=1,25\)
=> \(\left\{{}\begin{matrix}\%V_{NH_3}=20\%\\\%V_{N_2}=\dfrac{9-1,25}{9-1,25+6-1,25.3+2.1,25}.100\%=62\%\\\%V_{H_2}=\left(100-20-62\right)\%=18\%\end{matrix}\right.\)