Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Xử Lý hỗn hợp khí X: 3 khí đó chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2 và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa N2 và N2O với MTrung bình = 36 = MTrung bình cộng của 2 khí.
⇒ nN2 = nN2O || Đặt nNO = a và nN2 = nN2O = b ta có hệ:
a + 2b = 0,04 || 30a + 28b + 44b = 1,32 ||⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận = 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là x và y ta có hệ:
(24+17×2)x + (27+17×3)y = 6,42 || 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol ⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ ⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2 = 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15 = 0,345 mol.
⇒ mDung dịch HNO3 = 0 , 345 × 63 × 100 24 = 90,5625 gam

Đặt công thức trung bình 2 ancol là CnH2n+1OH, công thức trung bình 3 ete là (CnH2n+1)2O, phân tử khối trung bình 3 ete là 6,76/0,08 = 84,5. Do đó: 28n + 18 = 84,5 suy ra n = 2,375. Vì vậy, 2 ancol cần tìm là C2H5OH (a mol) và C3H7OH (b mol).
Để đốt cháy hoàn toàn Z cần một lượng O2 đúng bằng lượng cần dùng để đốt cháy T:
C2H6O + 3O2 \(\rightarrow\) 2CO2 + 3H2O
C3H8O + 9/2O2 \(\rightarrow\) 3CO2 + 4H2O
Nên ta có: 40a + 60b = 27,2 và 3a + 4,5b = 43,68/22,4 = 1,95. Tính được: a = 0,2 và b = 0,3 mol.
Gọi x, y tương ứng là số mol ancol tạo ete, ta có: x + y = 2.0,08 = 0,16 và 46x + 60y = 6,76 + 18.0,02 = 8,2.
Thu được: x = 0,1 và y = 0,06 mol.
Do đó, hiệu suất tạo ete của X = 0,1/0,2 = 50%; của Y = 0,06/0,3 = 20%.

Đáp án A
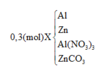
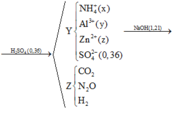
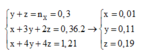
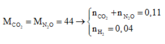
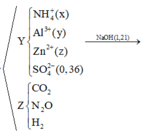
n C O 2 = a n N 2 O = b → a = 0 , 07 b = 0 , 04
B T N T ( N ) : n A l ( N O 3 ) 3 = x + 2 b 3 = 0 , 03
![]()
B T N T ( C ) : n Z n C O 3 = a = 0 , 07
B T N T ( Z n ) : n Z n ( X ) = z - a = 0 , 12
⇒ % = 8 , 61

Đáp án C
Xử lí dữ kiện Z: Bảo toàn khối lượng:
![]() = 6,12 gam
= 6,12 gam
→![]() gam →
gam →
![]() mol
mol
→ ![]() gam →
gam →
![]() mol.
mol.
![]()
![]() gam
gam
![]() mol
mol
![]()
![]()
Ta có phản ứng Dumas: -COONa + NaOH → -H + Na2CO3 (vôi tôi xút).
![]()
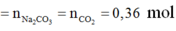
![]()
![]()
K gồm 2 khí trong đó có CH4.
Mà sau khi dẫn qua dung dịch Br2 dư chỉ còn 1 khí thoát ra
⇒ khí còn lại bị hấp thụ.
![]()
trong A chứa 2 gốc CH3COO-
⇒ gốc còn lại cũng là gốc axit đơn chức
⇒ nkhí còn lại = nA = 0,12 mol.
⇒ Mkhí còn lại =
![]()
khí còn lại là C2H4.
⇒ là (CH3COO)2(CH2=CH-COO)C3H5
⇒ a = 0,12 . 230 = 2,76
![]() mol
mol
⇒ x = 0,38 ÷ 0,19 = 2.
Muối gồm 0,12 mol
![]() ;
;
0,24 mol CH3COONa; 0,02 mol NaCl
=> b = 0,12.94 + 0,24.82 + 0,02.58,5 = 32,13
=> a + b + x = 61,73 gam

Đáp án C
Ta có: MX < 160
Cho 13,8 gam X tác dụng với NaOH được dung dịch cô cạn thu được rắn Y có khối lượng 22,2 gam.
Đốt cháy Y thu được 0,15 mol Na2CO3 và hỗn hợp khí Z.
Dẫn Z qua bình nước vôi trong thu được 0,25 mol kết tủa CaCO3 và dung dịch T.
Đun dung dịch thu được thêm 0,15 mol kết tủa nữa.
Do vậy T chứa 0,15 mol Ca(HCO3)2
→ n C O 2 = 0 , 25 + 0 , 15 . 2 = 0 , 55 m o l
Dung dịch thu được có khối lượng tăng lên so với ban đầu là 3,7 gam
→ m C O 2 + m H 2 O - m C a C O 3 = 3 , 7 → n H 2 O = 0 , 25 m o l
Bảo toàn nguyên tố Na suy ra số mol NaOH là 0,3 mol.
Bảo toàn khối lượng: m H 2 O = 13 , 8 + 0 , 3 . 40 - 22 , 2 = 3 , 6 → n H 2 O = 0 , 2
Bảo toàn nguyên tố C: nO trong X = 0,55 + 0,15 = 0,7 mol
Bảo toàn nguyên tố H: nH trong X = 0,25.2 + 0,2.2-0,3 = 0,6 mol
=> n O t r o n g X = 13 , 8 - 0 , 7 . 12 - 0 , 6 16 = 0 , 3
Do vậy trong X tỉ lệ C:H:O=7:6:3 nên CTPT của X có dạng (C7H6O3)n
mà theo giả thiết đầu nên n phải bằng 1.
Vậy X là C7H6O3.
=> nX =0,1 mol
Vậy X tác dụng với NaOH theo tỉ lệ 1:3 và sinh ra 2H2O nên CTCT của X dạng HCOOC6H4OH.
X tác dụng được với nước brom vừa đủ sẽ tạo thành HO-CO-O-C6H4-x(OH)(Br)x
→ 80 x 61 + 12 . 6 + 4 x + 17 + 80 x = 51 , 282 % → x = 2 như vậy sẽ chỉ có 2Br được thế nằm ở trên vòng.ư
Do đó vị trí của nhóm chức HCOO- trên vòng so với HO- là sẽ ở vị trí o hoặc p.
Do vậy có 2 đồng phân cấu tạo phù hợp với X.

Đáp án là C
Ta có
mX=13.8 , MX <160
X + NaOH thu được Y
Y + O2 => ![]() = 0.15
= 0.15
=> nNaOH =0.3 và Z
Z + Ca(OH)2 ta có phương trình:
m tăng thêm + m kết tủa 1= 28.7 g
= ![]()
Tổng mol 2 lần kết tủa là 0.55 = số mol của CO2
=> nC trong X= 0.55+0.15=0.7 mol
Suy ra mol H2O = 0.25 mol
Ta có phương trình
X + NaOH ![]() Y + H2O
Y + H2O
Bảo toàn khối lượng
![]() = 0.2 mol
= 0.2 mol
Bảo toàn H ta có
nH trong X = 0.2*2+ 0.25*2 – 0.3= 0.6 mol
Suy ra ta tính được nO trong X=( 18.96-0.6-0.7*12) /16= 0.3
Suy ra công thức đơn giản nhất trùng với công thức phân tử của X là C7H6O3
Do X tác dụng với Br2 ra % Br=51.282% ứng với công thức C7H4O3Br2
X có 4 π trong phân tử và tác dụng với 3 mol NaOH nên X là este của HCOOH với C6H4(OH)2
Suy ra công thức cấu tạo X được 2 cái ( OH ở vị trí octo hoặc para vì chỉ tác dụng được với 2 Br2)

Đáp án C
![]()
CO2 + dung dịch NaOH
NaOH + CO2 → NaHCO3 (1)
2NaOH + CO2 → Na2CO3 + H2O (2)
BaCl2
+ Na2CO3 → BaCO3↓ + 2NaCl
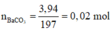
![]()
![]()
Dung dịch Z + dung dịch KOH
2NaHCO3 + 2KOH → K2CO3 + Na2CO3 + 2H2O
![]()
![]()
![]()
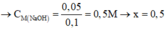
![]()
Từ phương trình (*) → m M g C O 3 p h ả n ứ n g = 0,03.84 = 2,52 g
→ Hiệu suất phản ứng là:
![]()

Chọn đáp án A.
38 g C 2 H 5 CHO : a m o l RCH 2 OH : b mol R ' COOCH 2 R : c mol → O X C 2 H 5 COOH : a mol RCOOH : b mol R ' COOCH 2 R : c mol
Có a + b + c = n N a O H − n H C l = 0 , 5.1 , 5 − 0 , 15 = 0 , 6 (1)
Chất E là RCH2OH ⇒ F là (RCH2)2O
⇒ 2 R + 44 R + 31 = 1 , 61 ⇒ R = 15 (-CH3)
m m u o i = m C 2 H 5 C O O N a + m C H 3 C O O N a + m R ' C O O N a + m N a C l ⇒ 96 a + 82 b + R ' + 67 c + 58 , 5.0 , 15 = 62 , 775 ( 2 ) m X = 58 a + 46 b + R ' + 73 c = 38 g ( 3 )
Thử đáp án:
R ' = C 3 H 5 − ⇒ a = 0 , 0875 b = 0 , 375 c = 0 , 1375 ⇒ Thỏa mãn
R ' = C 4 H 7 − ⇒ a = − 0 , 034 b = 0 , 502 c = 0 , 132 ⇒ Loại
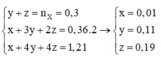
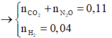
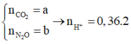
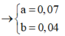
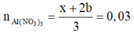
Đáp án D