Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Xét 2TH
TH1:19,6g là Cu(OH)2.Ta tìm ra kim loại là Ca
TH2:19,6g là Cu(OH)2 và RSO4(TH này loại)

\(a,PTHH:2Na+2H_2O\rightarrow2NaOH+H_2\\ n_{Na}=\dfrac{2,3}{23}=0,1mol\\ n_{NaOH}=0,1.2=0,2mol\\ C_{M_{NaOH}}=\dfrac{0,2}{0,5}=0,4M\\ b,oxit.kl:RO\\ n_{RO}=\dfrac{2,4}{R+16}mol\\ n_{HCl}=\dfrac{30.7,3}{100.36,5}=0,06mol\\ RO+2HCl\rightarrow RCl_2+H_2O\\ \Rightarrow\dfrac{2,4}{R+16}=0,06:2\\ \Leftrightarrow R=64,Cu\)

R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)

\(n_{CuSO_4}=\dfrac{15,2}{160}=0,095mol\\ CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
0,095 0,19 0,095 0,095
\(m_{rắn}=m_{Cu\left(OH\right)_2}=0,095.98=9,31g\\ V_{ddNaOH}=\dfrac{0,19}{2}=0,095l\\ b)C_{M_{Na_2SO_4}}=\dfrac{0,095}{0,04+0,095}\approx0,7M\\ c)Cu\left(OH\right)_2\xrightarrow[t^0]{}CuO+H_2O\)
0,095 0,095
\(m_{rắn}=m_{CuO}=0,095.80=7,6g\)

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
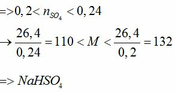
b)
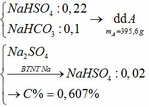
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O

Ta có: \(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)\)
a. PTHH: 2Na + 2H2O ---> 2NaOH + H2↑
b. Ta có: \(n_{H_2O}=\dfrac{97,8}{18}=5,43\left(mol\right)\)
Ta thấy: \(\dfrac{0,1}{2}< \dfrac{5,43}{2}\)
=> H2O dư.
Theo PT: \(n_{H_2}=\dfrac{1}{2}.n_{Na}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
=> \(V_{H_2}=0,05.22,4=1,12\left(lít\right)\)
c. Ta có: \(m_{dd_{NaOH}}=2,3+97,8=100,1\left(g\right)\)
Theo PT: \(n_{NaOH}=n_{Na}=0,1\left(mol\right)\)
=> \(m_{NaOH}=0,1.40=4\left(g\right)\)
=> \(C_{\%_{NaOH}}=\dfrac{4}{100,1}.100\%=3,996\%\)





TH 19,6 gam là Cu(OH)2 biết rồi
TH 19,6 gam là Cu(OH)2 và RSO4 thì chưa biết
trình bày cụ thể giúp ạ
mk chx hok phần này bn nhé