Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chú ý: Mỗi lần hỏi bạn up lên từng câu hỏi thôi, không nên đưa một lúc nhiều câu hỏi trong 1 lần hỏi, vì như thế chỉ có 1 câu được trả lời thôi nhé.
HD:
Bài 1.
Vì Cu đứng sau H trong dãy các kim loại nên Cu không phản ứng với HCl.
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
0,075 mol
Theo phản ứng trên, số mol Fe = số mol H2 = 0,075 mol. Suy ra khối lượng Fe = 56.0,075 = 4,2 g.
Khối lượng Cu = 8 - 4,2 = 3,8 g. Từ đó, %Fe = 4,2.100/8 = 52,5%; %Cu = 100 - 52,5 = 47,5%.

bảo toàn khối lượng ta có: 8,66+6,48+\(m_{khí}\)=28,99

Đáp án B
Chú ý: Có H2 nên N O 3 - đã hết; N2O không tác dụng với O2.


Đáp án A
Xử lý hỗn hợp khí X: 3 khí đó
chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2
và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa
N2 và N2O với
MT.bình = 36 = MT.bình cộng của 2 khí.
⇒ nN2 = nN2O
Đặt nNO = a và nN2 = nN2O = b
Ta có hệ:
a + 2b = 0,04
& 30a + 28b + 44b = 1,32
⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận
= 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là
x và y ta có hệ:
(24+17×2).x + (27+17×3)y = 6,42
& 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol
⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ
⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2
= 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15
= 0,345 mol
⇒ mDung dịch HNO3 = 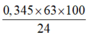
= 90,5625 gam

Đáp án : D
.nX = 0,3 mol ; nZ = 0,2 mol
Chỉ có NO phản ứng với O2 tạo NO2 bị hấp thụ vào nước
=> nNO = 0,3 – 0,2 = 0,1 mol
MZ= 40g (Z gồm N2 và N2O )
=> nN2 = 0,05 mol ; nN2O = 0,15 mol
.m(g) P : Mg,Al -> Kết tủa lớn nhất : Mg(OH)2 ; Al(OH)3 : (m + 39,1)g
=> mOH = (m + 39,1) – m = 39,1g => nOH = 2,3 mol = 2nMg + 3nAl
Lại có : nMg : nAl = 4 : 5 => nMg = 0,4 mol ; nAl = 0,5 mol
Bảo toàn e : 2nMg + 3nAl = 10nN2 + 8nN2O + 3nNO + 8nNH4NO3
=> nNH4NO3 = 0,0375 mol
=> Bảo toàn N : nHNO3 pứ = 2nMg + 3nAl + 2nN2 + nNO + 2nN2O + 2nNH4NO3
=> nHNO3 pứ = 2,875 mol
=> nHNO3 đầu = 3,45 mol => mdd HNO3 = 1086,75g
=> mdd sau = mP + mdd HNO3 - mkhí = 1098,85g
=> %CAl(NO3)3 = 9,69%

PTK trung bình của hỗn hợp NO và N2O = 18,5 x 2 = 37
--> n NO = n N2O = 4,48/44,8 = 0,1 mol
--> n HNO3 = 1,1(0,1 x 4 + 0,1 x 10) = 1,54 mol
--> Cm HNO3 = 1,54/2 = 0,77 lít = 770 ml.
m muối = 13,4 + 0,1 x 3 x 62 + 0,1 x 8 x 62 = 81,6 gam.

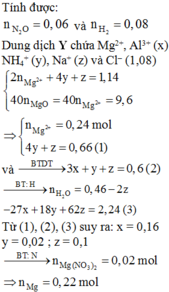
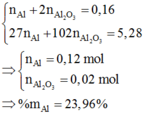




a) Giả sử axit hết :3
Gọi số mol của \(Mg\) và \(Al\) lần lựơt là x và y \(mol\)=>mhh ban đầu=24x+27y=3,87g
\(Mg+2HCl\rightarrow MgCl2+H2\)
x \(\text{mol}\)=>2x \(\text{mol}\) =>x \(\text{mol}\)
2\(Al\) + 6\(HCl\) => 2\(AlCl3\) + 3\(H2\)
y \(\text{mol}\) =>3y \(\text{mol}\) =>1,5y \(\text{mol}\)
\(\text{mol}\) \(HCl\)=0,5 \(\text{mol}\)=>2x+3y=0,5
giải ra âm=>GS vô lí=>axit \(HCl\) còn dư
b) mol\(H2\) =0,195 \(\text{mol}\)
=>x+1,5y=0,195
kết hợp vs pt số gam hh giải ra x=0,06\(\text{mol}\) ;y=0,09 \(\text{mol}\) =>m\(Mg\)=1,44g,m\(Al\)=2,43g
c) mol \(HCl\) =2mol\(H2\)=0,195.2=0,39\(mol\)
=>mol \(H\)+ dư = mol \(HCl\) dư=0,5-0,39=0,11 \(\text{mol}\)
Gọi thể tích dung dịch là V(l)
mol NaOHNaOH=2V molmol
mol Ba(OH)2Ba(OH)2=0,1V molmol
do \(NaOH\) và \(Ba\left(OH\right)2\) là các hiđroxit mạnh pli hoàn toàn ra \(OH\)-
số mol \(OH\)- trong dung dịch =2V+0,1.2V=2,2V \(\text{mol}\)
pt ion
\(H++OH-\Rightarrow H2O\)
0,11 \(\text{mol}\) =>0,11 \(\text{mol}\)
=>0,11=2,2V=>V=0,05(l)