Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
PTHH: S + O2 ==to==> SO2
a/ nS = 3,2 / 32 = 0,1 mol
nSO2 = nS = 0,1 (mol)
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
b/ nO2 = nS = 0,1 mol
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
Mà không khí gấp 5 lần thể tích oxi
=> Thể tích không khí cần dùng là: 2,24 . 5 = 11,2 (lít)
Câu 3: Ta có \(\frac{d_A}{H_2}\)= 8
=> MA = MH2 . 8 = 2 . 8 = 16 g
mH = \(\frac{25\%.16}{100\%}\)= 4 g
mC = \(\frac{75\%.16}{100\%}\)= 12 g
nH = 4 mol
nC = 1 mol
CTHH : CH4

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, \(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,3}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe_2O_3\left(pư\right)}=\dfrac{1}{3}n_{H_2}=0,1\left(mol\right)\Rightarrow n_{Fe_2O_3\left(dư\right)}=0,3-0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,2.160=32\left(g\right)\)

\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_{HCl}=\dfrac{m}{M}=\dfrac{18,25}{1+35,5}=0,5\left(mol\right)\\ PTHH:Fe+2HCl->FeCl_2+H_2\)
tỉ lệ 1 : 2 : 1 : 1
n(mol) 0,2------->0,4--------->0,2---->0,2
\(\dfrac{n_{Fe}}{1}< \dfrac{n_{HCl}}{2}\left(\dfrac{0,2}{1}< \dfrac{0,5}{2}\right)\)
`=> Fe` hết, `HCl` dư, tính theo `Fe`
\(n_{HCl\left(dư\right)}=0,5-0,4=0,1\left(mol\right)\\ m_{HCl\left(dư\right)}=n\cdot M=0,1\cdot\left(1+35,5\right)=3,65\left(g\right)\\ V_{H_2\left(dktc\right)}=n\cdot22,4=0,2\cdot22,4=4,48\left(l\right)\)
a) Ta có : PTHH : \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có : \(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{m}{M}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
Theo PTHH thì ta có : \(2n_{Fe}=n_{HCl}\)
Giả sử HCl dùng hết : \(\Rightarrow n_{Fe}\) cần dùng là : \(0,25\left(mol\right)\) không thỏa mãn
\(\Rightarrow Fe\) dùng hết ; HCl dư
Số mol HCl dư là :
\(0,5-0,2.2=0,1\left(mol\right)\)
Khối lượng dư của HCl là :
\(0,1.36,5=3,65\left(g\right)\)
b) Do Fe dùng hết nên ta tính H theo Fe
Theo PTHH : \(n_{Fe}=n_{H_2}\)
\(\Rightarrow n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

a.b.c.\(n_{Al}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 0,1 0,15 ( mol )
\(V_{H_2}=0,15.22,4=3,36l\)
\(m_{AlCl_3}=0,1.133,5=13,35g\)
d.\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,15 0,1 ( mol )
\(m_{Fe}=0,1.56=5,6g\)

Câu 1:
PTHH: Fe + 2HCl ===> FeCl2 + H2
a/ nFe = 11,2 / 56 = 0,2 mol
=> nH2 = 0,2 mol
=> VH2(đktc) = 0,2 x 22,4 = 4,48 lít
b/ => nHCl = 0,2 x 2 = 0,4 mol
=> mHCl = 0,4 x 36,5 = 14,6 gam
c/ => nFeCl2 = 0,2 mol
=> mFeCl2 = 0,2 x 127 = 25,4 gam
Câu 3/
a/ Chất tham gia: S, O2
Chất tạo thành: SO2
Đơn chất: S, O2 vì những chất này chỉ do 1 nguyên tố tạo nên
Hợp chất: SO2 vì chất này do 2 nguyên tố S và O tạo tên
b/ PTHH: S + O2 =(nhiệt)==> SO2
=> nO2 = 1,5 mol
=> VO2(đktc) = 1,5 x 22,4 = 33,6 lít
c/ Khí sunfuro nặng hơn không khí

\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
a)\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6 0,3
\(C_M=\dfrac{0,6}{0,4}=1,5M\)
b)\(n_{CuO}=\dfrac{32}{80}=0,4mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,4 0,3 0,3
Sau phản ứng CuO dư và dư \(\left(0,4-0,3\right)\cdot80=8g\)
\(m_{rắn}=m_{Cu}=0,3\cdot64=19,2g\)

a) \(n_{Fe_2O_3}=\frac{32}{160}=0,2\left(mol\right)\)
PTHH : \(Fe_2O_3+3H_2-t^o->2Fe+3H_2O\)
Theo pthh : \(n_{H_2}=3n_{Fe_2O_3}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6\cdot22,4=13,44\left(l\right)\)
b) Theo pthh : \(n_{H_2O}=n_{H_2}=0,6\left(mol\right)\)
=> \(m_{H_2O}=0,6\cdot18=10,8\left(g\right)\)
c) Theo pthh : \(n_{Fe}=2n_{Fe_2O_3}=0,4\left(mol\right)\)
=> \(m_{Fe}=0,4\cdot56=22,4\left(g\right)\)


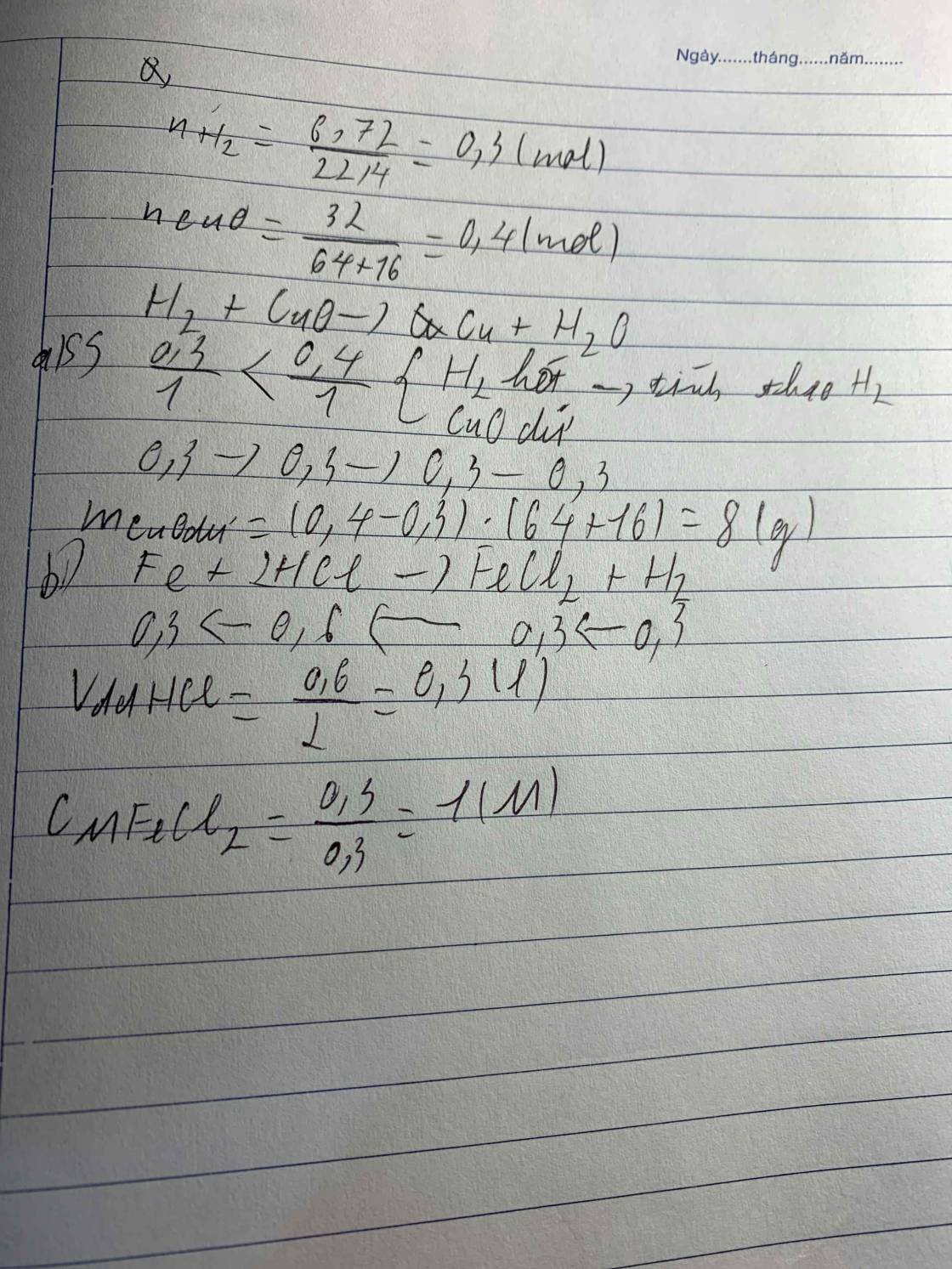
a. \(n_{Al}=\frac{m}{M}=\frac{2,7}{27}=0,1mol\)
PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,1 0,15 mol
\(\rightarrow n_{H_2}=n_{Al}=\frac{3.0,1}{2}=0,15mol\)
\(\rightarrow V_{H_2\left(ĐKTC\right)}=n.22,4=0,15.22,4=3,36l\)
b. \(n_{Fe_2O_3}=\frac{m}{M}=\frac{6,4}{160}=0,04mol\)
\(Fe_2O_3+3H_2\rightarrow^{t^o}2Fe+3H_2O\)
Ban đầu: 0,04 0,15 mol
Trong pứng: 0,04 0,12 mol
Sau pứng: 0 0,03 mol
Vậy sau phản ứng thì \(H_2\) dư và \(Fe_2O_3\) hết
\(\rightarrow m_{H_2\left(\text{dư}\right)}=n.M=0,03.2=0,06g\)