Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích:
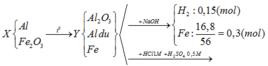
BT e: nAl dư = 2/3 nH2 = 2/3. 0,15 = 0,1 (mol)
BTNT: Fe => nFe2O3 = ½ nFe = 0,15 (mol)
Phản ứng xảy ra hoàn toàn, Al dư sau phản ứng ( vì Y + NaOH có khí H2 bay ra), do đó Fe2O3 phản ứng hết
Fe2O3 + 2Al Al2O3 + 2Fe
0,15 → 0,3
=> nAl ban đầu = 0,3 + 0,1 = 0,4 (mol)
nHCl = V (mol) ; nH2SO4 = 0,5V (mol)
Bảo toàn điện tích khi cho Y tác dụng với hh axit
=> 2nFe2+ + 3nAl3+ = nCl- + 2nSO42-
=> 2.0,3 + 3. 0,4 = V + 2. 0,5V
=> V = 0,9 (lít)
Đáp án B

Đáp án D
2Al + 6H+ → 2Al3+ + 3H2
0,1 ←0,3 ← 0,15
[Al(OH)4]- + 4H+→ Al3+ + 4H2O
0,125 ← (0,8 – 0,3)
Al + OH- + 3H2O →[Al(OH)4]- + 3/2 H2
0,125 ← 0,125 ← 0,125
⇒ m = (0,125 + 0,1).27 = 6,075 g
⇒V dd NaOH = 0,125/ 2 = 0,0625 lít

Đáp án D
nH+ (1) = nH+ (2) ⇒ 4V1 = V2 (3+1.2) ⇒V1 = 1,25V2

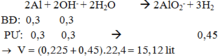
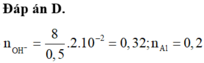
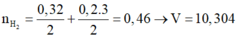
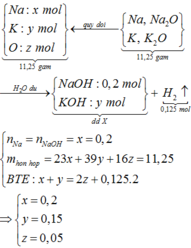
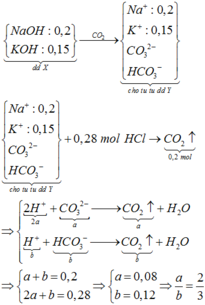
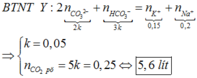
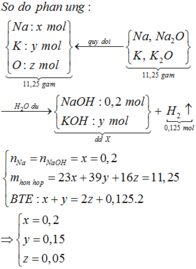
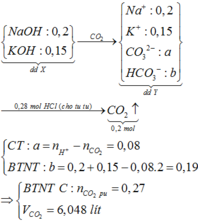

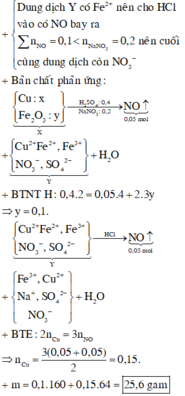
Đây là bài tập về phản ứng của kim loại với dung dịch có chứa và OH-, áp dụng phần lí thuyết ta viết được các phương trình phản ứng:
Do đó V 1 < V < V 2 . Quan sát các đáp án ta được đáp án đúng là B.
Đáp án B.