Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học của phản ứng:
M + n/2HCl → M Cl n
M + mHCl → M Cl m + m/2 H 2
Theo đề bài, ta có:
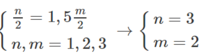
và M + 106,5 = 1,2886 (M+71)
Giải ra, ta có M = 52 (Cr)

Bài 1:
PTHH: \(CH_4+Cl_2\underrightarrow{a/s}CH_3Cl+HCl\)
Theo PTHH: \(n_{Cl_2}=n_{CH_3Cl}=n_{CH_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CH_3Cl}=0,15\cdot50,5=7,575\left(g\right)\\V_{CH_4}=V_{Cl_2}=3,36\left(l\right)\end{matrix}\right.\)
Bài 2:
PTHH: \(CH_4+2O_2\underrightarrow{a/s}CO_2+2H_2O\)
Theo PTHH: \(\left\{{}\begin{matrix}n_{CO_2}=n_{CH_4}\\n_{O_2}=2n_{CH_4}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{CO_2}=V_{CH_4}=5,6\left(l\right)\\V_{CO_2}=2V_{CH_4}=11,2\left(l\right)\end{matrix}\right.\)

Gọi số mol KMnO4 và KClO3 trong hỗn hợp ban đầu lần lượt là x,y
158x + 122,5y= 48,2 (1)
Bảo toàn elcton toàn quá trình ta có
Mn+7+5e →Mn+2
x 5x
Cl+5 + 6e → Cl–1
y 6y
(về bản chất có 1 phần Cl+5 có 1 phần chuyển sang Cl0, nhưng Cl–1 lại nhường e tạo Cl0 vì vậy để đơn giản ta có thể coi tất cả Cl+5 tạo thành Cl–1)
2Cl–1→ Cl2 +2e
0,675 0,135
2O–2 → O2 + 4e
0,15 0,6
Áp dụng định luật bảo toàn e ta có 5x+6y=1,95 (2)
Từ 1 và 2 ta có hệ phương trình
Giải ta được x=0,15 và y=0,2
% mKMnO4 = 49,17 % và % mKClO3 =50,83%

PTHH: \(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{MnO_2}=\dfrac{17,4}{87}=0,2\left(mol\right)\\n_{HCl}=0,5\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,5}{4}\) \(\Rightarrow\) MnO2 còn dư, tính theo HCl
\(\Rightarrow n_{Cl_2}=0,125\left(mol\right)\) \(\Rightarrow V_{Cl_2}=0,125\cdot22,4=2,8\left(l\right)\)
Cho 4,8g khí Metan tác dụng với khí Clo ở điều kiện thích hợp. Khối lượng Metyl clorua thu được là ?

\(n_{CH_4}=\dfrac{m}{M}=0,3\left(mol\right)\)
\(CH_4+Cl_2\rightarrow CH_3Cl+HCl\)
.0,3....................0,3...........
\(\Rightarrow m_{CH3Cl}=n.M=15,15\left(g\right)\)

a) Bảo toàn nguyên tố H : \(n_{HCl}.1=2n_{H_2}=0,6\left(mol\right)\)
=> nH2=0,3(mol)
=> \(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b) Áp dụng định luật bảo toàn khối lượng :
\(m_{ct}=m_{kl}+m_{HCl}-m_{H_2}=10,4+0,6.36,5-0,3.2=31,7\left(g\right)\)

Trong hai khí trên, chỉ có khí etilen tác dụng với dung dịch nước brom, khối lượng bình tăng bằng khối lượng khí etilen tham gia phản ứng, suy ra số mol của khí etilen là 2,8/28=0,1 (mol).
Khí đem đốt cháy là khí metan, số mol khí metan bằng số mol khí CO2 sinh ra (bảo toàn nguyên tố cacbon) và bằng 11/44=0,25 (mol).
a. Giá trị V=(0,25+0,1).22,4=7,84 (lít).
b. Phần trăm thể tích mỗi khí:
%Vmetan=0,25/0,35.100%\(\approx\)71,43%, suy ra %Vetilen\(\approx\)100%-71,43%\(\approx\)28,57%.

có: nCH4= \(\dfrac{2,24}{22,4}\)= 0,1( mol)
PTPU
CH4+ Cl2\(\xrightarrow[]{as}\) CH3Cl+ HCl
0,1......0,1..........0,1............. mol
\(\Rightarrow\) mCH3Cl= 0,1. 50,5= 5,05( g)
\(\Rightarrow\) mA= \(\dfrac{5,05}{100\%-83,53\%}\)= 30,66( g)
\(\Rightarrow\) mCl2= 30,66. 83,53%= 25,61( g)
\(\Rightarrow\) \(\sum nCl2\)= \(\dfrac{25,61}{71}\)+ 0,1= 0,46( mol)
\(\Rightarrow\) VCl2= 0,46. 22,4= 10,304( lít)