Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

gọi a, là số mol của Mg và Fe
PTHH: 2Mg+O2=>2MgO
a------a/2------>a
2Fe+O2=>2FeO
b--------b/2----->b
theo đề ta có hpt: \(\begin{cases}40a+68b=12\\24a+56b=8\end{cases}\)
<=>\(\begin{cases}a=\frac{4}{19}\\b=\frac{1}{19}\end{cases}\)
=> V=(4/19+1/19).22,4=5,9ml
mMg=4/19.24=5,1g
=> %Mg=\(\frac{5,1}{8}.100=63,75\%\)
%Fe=100-63,75=36,25%

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Gọi số mol O2 pư là x (mol)
2H+1 + 2e --> H20
0,8<--0,4
O20 + 4e --> 2O-2
x---->4x
=> 4x = 0,8
=> x = 0,2 (mol)
=> m = 15 + 0,2.32 = 21,4 (g)

Đáp án A
Bảo toàn electron có:
2. n F e = 2 . n k h í → n F e = n k h í = 0,1 mol.
m F e = 0,1.56 = 5,6 gam.

Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
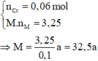
=> a = 2, M = 65 (M là Zn).

Đáp án D
Đặt Zn, Cr,Sn là x mol → ZnCl2 : x mol, SnCl2 : x mol và CrCl2 : x mol
→ x =0,02 mol
Bảo toàn O trong phương trình đốt cháy có 2nO2 = x + 2x + 3/2 x =0,09
→ VO2= 1,008 lít

Đáp án B
n H 2 = 0 , 1 ; n NO = 0 , 4 . Gọi n là hóa trị của M.
Căn cứ vào 4 đáp án ta có 2 trường hợp:
+) M là kim loại đứng trước H trong dãy hoạt động hóa học. Khi đó cả M và Fe có phản ứng với dung dịch HCl. Vì hóa trị của M không đổi nên sự chênh lệch về số electron trao đổi trong hai lần thí nghiệm là do sắt có hai mức hóa trị là II và III.
Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có: 2 n Fe + n . n M = 2 n H 2
- Khi hòa tan hỗn hợp vào dung dịch HNO3, ta có: 3 n Fe + n . n M = 3 n NO
Trừ hai vế của hai phương trình cho nhau, ta được:
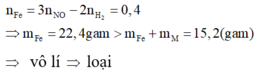
+) M là kim loại đứng sau H và trước Pt trong dãy hoạt động hóa học. Khi đó M không phản ứng được với dung dịch HCl và phản ứng được với dung dịch HNO3. Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có:


Đáp án C
Các phản ứng xảy ra:
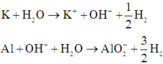
Vì hai trường hợp có khối lượng hỗn hợp đem hòa tanlà như nhau mà thể tích H2 thu được khác nhau nên khihòa tan hỗn hợp vào nước, một phần Al dư đã khôngtan. Gọi nK = a; nAl = n có:
+ Khi hòa tan vào nưóc dư: ![]()
+ Khi hòa tan vào dd NaOH dư: ![]()
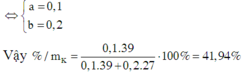
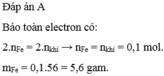

n02=0,1mol
PThh: 4Al+3O2=>2Al2O3
2/15<-0,1->1/15
=> mAl2O3=1/15.102=6,8g
OK chứ ??
2Al + 3O2 ----> 2Al2O3
nO2=2,24/22,4=0.1mol
nAl2O3=nO2=0,1 mol
----> mAl2O3=0,1*102=10.2g