Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

C đúng
nH2 = 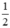 = 0,5 mol.
= 0,5 mol.
Mg + 2HCl → MgCl2 + H2
Fe + 2HCl → FeCl2 + H2
nMg = x; nFe = y.
nH2 = x + y = 0,5 mol.
mhh = 24x + 56y = 20g.
Giải hệ phương trình ta có x = y =0,25 mol.
mMgCl2 = 0, 25 × 95 = 23,75g.
mFeCl2 = 0,25 × 127 = 31,75g
Khối lượng muối clorua = 23,75 + 31,75= 55,5

a)
Zn + 2HCl → ZnCl2 + H2
Fe + 2HCl → FeCl2 + H2
b) Gọi số mol Zn và Fe có trong 17,7 gam hỗn hợp là x và y mol. nH2 = \(\dfrac{6,72}{22,4}\)=0,3 mol
Theo tỉ lệ phản ứng ta có \(\left\{{}\begin{matrix}x+y=0,3\\65x+56y=17,7\end{matrix}\right.\)=> x = 0,1 và y = 0,2
=> mZn = 0,1.65 = 6,5 gam và mFe= 0,2.56 = 11,2 gam
c) nHCl = 2nH2 = 0,3.2 = 0,6 mol
Áp dụng ĐLBT khối lượng => m muối clorua = mKl + mHCl - mH2
<=> m muối = 17,7 + 0,6.36,5 - 0,3.2 = 28,05 gam

\(n_{H2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
a 0,4 0,2 1a
\(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
b 0,3 0,15 1b
a) Gọi a là số mol của Mg
b là số mol của Fe
\(m_{Mg}+m_{Fe}=13,2\left(g\right)\)
⇒ \(n_{Mg}.M_{Mg}+n_{Fe}.M_{Fe}=13,2g\)
⇒ 24a + 56b = 13,2g (1)
Theo phương trình : 1a + 1b = 0,35(2)
Từ(1),(2), ta có hệ phương trình :
24a + 56b = 13,2g
1a + 1b = 0,35
⇒ \(\left\{{}\begin{matrix}a=0,2\\b=0,15\end{matrix}\right.\)
\(m_{Mg}=0,2.24=4,8\left(g\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
0/0Mg = \(\dfrac{4,8.100}{13,2}=36,36\)0/0
0/0Fe = \(\dfrac{8,4.100}{13,2}=63,64\)0/0
b) \(n_{HCl\left(tổng\right)}=0,4+0,3=0,7\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddHCl}}=\dfrac{0,7}{0,2}=3,5\left(M\right)\)
c) \(m_{muối.clorua}=\left(0,2.95\right)+\left(0,15.127\right)=38,05\left(g\right)\)
Chúc bạn học tốt

Gọi số mol của Fe và Mg trong hỗn hợp ban đầu là \(x,y\) mol.
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\left(1\right)\)
Số mol: \(x\left(mol\right)--->x\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\left(2\right)\)
Số mol: \(y\left(mol\right)--->y\left(mol\right)\)
Theo (1), ta có: \(n_{FeCl_2}=n_{Fe}=x\left(mol\right)\)
Theo (2), ta có: \(n_{MgCl_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow\)mmuối clorua = \(m_{FeCl_2}+m_{MgCl_2}\)
\(\Leftrightarrow24,2=127x+95y\left(3\right)\)
Có: mhỗn hợp kim loại ban đầu = mFe + mMg
\(\Leftrightarrow10=56x+24y\left(4\right)\)
Từ (3) và (4), ta có hệ: \(\left\{{}\begin{matrix}127x+95y=24,2\\56x+24y=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1625\\y=0,0375\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=0,1625.56=9,1\left(g\right)\)
\(\Rightarrow\%m_{Fe}=\dfrac{9,1}{10}.100\%=91\%\)
\(\Rightarrow\%m_{Mg}=100\%-91\%=9\%\)

\(\left\{{}\begin{matrix}Fe\\Al\end{matrix}\right.+HCl->\left\{{}\begin{matrix}FeCl2\\AlCl3\end{matrix}\right.+H2\)
Ta có số mol Fe là x , Al là y (mol)
\(\left\{{}\begin{matrix}56x+27y=11\\127x+133,5y=39,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%mFe=\dfrac{0,1.56}{11}=50,9\%\\\%mAl=\dfrac{0,2.27}{11}=49,09\%\end{matrix}\right.\)
Bảo toàn e :
\(2.nH2=2.nFe+3.nAl\Rightarrow nH2=0,4\left(mol\right)\)
\(V=0,4.22,4=8,96\left(l\right)\)
\(nFe=nFeCl2=0,1\left(mol\right)\)
\(nAl=nAlCl3=0,2\left(mol\right)\)
\(\Rightarrow nHCl\left(pứ\right)=2.0,1+3.0,2=0,8\left(mol\right)\)
\(Cm=\dfrac{n}{V}=\dfrac{0,8}{0,2}=4\left(M\right)\)

PTHH:
2Na + 2HCl ===> 2NaCl + H2
a------a--------------a
2K + 2HCl ===> 2KCl + H2
b------b------------b
Đặt số mol Na, K lần lượt là a, b (mol)
Lập các số mol trên phương trình, ta có hệ phương trình:
\(\left\{\begin{matrix}23a+39b=20\\58,5a+74,5b=55,5\end{matrix}\right.\)
Giải ra nghiệm âm
=> Đề sai. Bạn xem lại đề xong đăng câu hỏi nên nhé!