Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Ta có : \(n_{CO2}=\dfrac{V}{22,4}=0,1\left(mol\right)\)
\(BTNT\left(C\right):n_{MgCO3}=n_{CO2}=0,1\left(mol\right)\)
\(\Rightarrow m_{MgCO3}=n.M=8,4\left(g\right)\)
\(\Rightarrow m_{MgO}=8\left(g\right)\)
b, Thấy sau khi phản ứng xảy ra thu được dung dịch A gồm \(MgSO_4\) và có thể còn \(H_2SO_4\) dư .
\(BTNT\left(Mg\right):n_{MgSO_4}=n_{MgCO3}+n_{MgO}=0,3\left(mol\right)\)
\(PTHH:MgSO_4+Ba\left(OH\right)_2\rightarrow Mg\left(OH\right)_2\downarrow+BaSO_4\downarrow\)
.................0,3............0,3..................0,3..................0,3.............
\(\Rightarrow m_{\downarrow}=m_{Mg\left(OH\right)2}+m_{BaSO4}=87,3\left(g\right)\)
Mà \(\left\{{}\begin{matrix}m\downarrow=110,6\left(g\right)>87,3g\\n_{Ba\left(OH\right)2}=C_M.V=0,45>n_{Ba\left(OH\right)2pu}\left(0,3mol\right)\end{matrix}\right.\)
=> Dung dịch A vẫn còn H2SO4 dư và mol BaSO4 được tạo ra tiếp là :
\(n_{BaSO4}=\dfrac{110,6-87,3}{M}=0,1\left(mol\right)\)
\(PTHH:H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
..................0,1............0,1...............0,1........................
Lại có : \(n_{Ba\left(OH\right)2}=0,45\left(mol\right)\)
=> Trong dung dịch B còn có Ba(OH)2 dư ( dư 0,45 - 0,3 - 0,1 = 0,05mol)
\(\Rightarrow C_{MBa\left(OH\right)2}=\dfrac{n}{V}=\dfrac{0,05}{0,5}=0,1\left(M\right)\)
Vậy ...

Ta có: \(n_{Na_2SO_3}=\dfrac{12,6}{126}=0,1\left(mol\right)\)
a. PTHH: Na2SO3 + 2HCl ---> 2NaCl + SO2 + H2O
Theo PT: \(n_{SO_2}=n_{Na_2CO_3}=0,1\left(mol\right)\)
=> \(V_{SO_2}=0,1.22,4=2,24\left(lít\right)\)
b. Theo PT: \(n_{HCl}=2.n_{SO_2}=2.0,1=0,2\left(mol\right)\)
=> \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
=> \(C_{\%_{HCl}}=\dfrac{7,3}{150}.100\%=4,87\%\)
c. Ta có: \(m_{dd_{NaCl}}=n_{Na_2SO_{3_{PỨ}}}=50\left(g\right)\)
Theo PT: \(n_{NaCl}=n_{HCl}=0,2\left(mol\right)\)
=> \(m_{NaCl}=0,2.58,5=11,7\left(g\right)\)
=> \(C_{\%_{NaCl}}=\dfrac{11,7}{50}.100\%=23,4\%\)

a) nMg= 3,6/24=0,15(mol)
nHCl= (300.7,3%)/36,5= 0,6(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
Ta có: 0,15/1 < 0,6/2
=> HCl dư, Mg hết => Tính theo nMg.
nY=nH2=nMgCl2=nMg=0,15(mol)
=>V(Y,đktc)=V(H2,đktc)=0,15.22,4=3,36(l)
b) mMgCl2=0,15.95= 14,25(g)
nHCl(dư)= 0,6- 0,15.2=0,3(mol)
=>mHCl(dư)=0,3.36,5= 10,95(g)
mddsau= mMg + mddHCl - mH2= 3,6+ 300 - 0,15.2= 303,3(g)
=>C%ddHCl(dư)= (10,95/303,3).100= 3,610%
C%ddMgCl2= (14,25/303,3).100=4,698%

1: \(n_{Zn}=\dfrac{3.25}{65}=0.05\left(mol\right)\)
a: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
0,05 0,1 0,05 0,05
\(m_{dd\left(HCl\right)}=0.1\cdot36.5=3.65\left(g\right)\)
b: \(V_{H_2}=0.05\cdot22.4=1.12\left(lít\right)\)
2)
H3PO4 (axit yếu) : axit photphoric
Zn3(PO4)2 (muối) : kẽm photphat
Fe2(SO4)3 (muối) : sắt (III) sunfat
SO2 (oxit axit) : lưu huỳnh đioxit
SO3 (oxit axit) : lưu huỳnh trioxit
P2O5 (oxit axit) : đi photpho pentaoxit
HCl(axit mạnh) : axit clohidric
Ca(HCO3)2 (muối axit) : canxi hidrocacbonat
Ca(H2PO4)2 (muối aixt) : canxi đihidrophotphat
Fe2O3 (oxit bazơ) : sắt (III) oxit
Cu(OH)2 (bazơ) : đống(II) hidroxit
NaH2PO4 (muối axit) : natri đihidrophotphat
Chúc bạn học tốt

a)X gồm Fe,Ag
\(Fe + 2AgNO_3 \to Fe(NO_3)_2 + Ag(1)\\ Fe + 2HCl \to FeCl_2 + H_2(2)\\ 2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(3)\\ 2Ag + 2H_2SO_4 \to Ag_2SO_4 + SO_2 + 2H_2O(4)\\\)
b) Phần 1,gọi n\(n_{Ag} = a(mol)\)
Theo PTHH (2) : \(n_{Fe} = n_{H_2} = 0,1(mol)\)
Suy ra : m2 = 0,1.56 + 108a = 5,6 + 108a(gam)
Phần 2, \(n_{Ag} = ak(mol) ; n_{Fe} = 0,1k(mol)\)
Theo PTHH (3)(4) : \(n_{SO_2} = \)0,5.ak + 0,1k.1,5 = 0,5ak + 0,15k = 0,4
⇒ k(0,5a + 0,15) = 0,4(1)
m3 = 108.ak + 0,1k.56 (gam)
Ta có :
\(m_3 - m_2 = 16,4 \Rightarrow m_3 = 16,4 + m_2\)
⇔ k(108a + 5,6) = 16,4 + 5,6 + 108a = 22+ 108a(2)
Ta lấy (1) : (2), ta có :
\(\dfrac{0,5a + 0,15}{108a + 5,6} = \dfrac{0,4}{22 + 108a}\)⇒ a = 0,1
Vậy : k = \(\dfrac{0,4}{0,5a + 0,15} = 2\)
Vậy X gồm :
Fe : 0,1 + 0,1.2 = 0,3(mol)
Ag : 0,1 + 0,1.2 = 0,3(mol)
Fe + 2AgNO3 →Fe(NO3)2 + 2Ag
0,3.....0,3...............................0,3.........(mol)
Vậy :
m = (0,3 + 0,3).56 = 33,6 gam
V = \(\dfrac{0,3}{1}\) = 0,3(lít)
phần tính a bạn giải chi tiết dùm mình dc không, mình giải ko ra

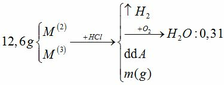
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
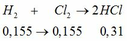
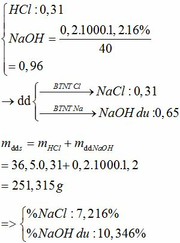



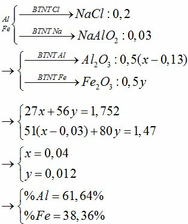
Chọn D
m d d s a u p ư = m c h ấ t t h a m g i a p ư – m H 2 → m d d s a u p ư = m Z n + m H C l – m H 2 = 16 , 25 + 300 – 0 , 25 . 2 = 315 , 75 g a m .