Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
![]()
![]()
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
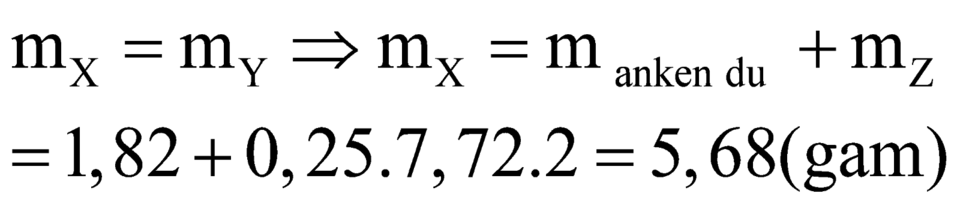
Mà ![]()
![]()
![]()
Do đó hai anken trong X là C2H4 và C3H6.
Cách 1: Áp dụng sơ đồ đường chéo hoặc giải hệ phương trình, ta có:
![]()
Cách 2: Ta có: ![]()
![]()
Vì ![]() nên
nên ![]()

Đáp án A
Vì nH2phản ứng = nanken phản ứng = nankan
→ nZ = nH2dư + nankan = nH2ban đầu = 0,25 mol.
→ nanken ban đầu = 0,4 - 0,25 = 0,15 mol.
Gọi x = nCnH2n + 2 → nH2dư = 0,25 - x (mol)
→ mZ = (14n + 2)x + 2(0,25 - x) = 0,25 x 7,72 x 2
→ 14nx = 3,36 (1)
nCnH2ndư = 0,15 - x → 14n(0,15 - x) = 1,82 (2)
Từ (1), (2) → x = 0,01; n = 2,47
→ C2H4 và C3H6.
• Đặt nC2H4 = a mol; nC3H6 = b mol.
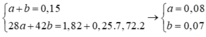
![]()

nBr2 = 0,05
Dẫn hỗn hợp Y qua dung dịch Br2 dư thấy khối lượng bình tăng 1,82 gam và có 8 gam brom đã tham gia phản ứng
⇒ nAnken/Y = nBr2 = 0,05 = nC2H4 dư + nC3H6 dư (1)
mAnken/Y = 1,82g
Vì Hiệu suất hidro hóa của 2 anken như nhau
⇒ nC2H4 phản ứng : nC2H4 ban đầu = nC3H6 phản ứng : nC3H6 ban đầu
⇒ nC2H4 dư : nC2H4 = nC3H6 dư : nC3H6
⇒ nC2H4 dư : 0,1 = nC3H6 dư : 0,15 (2)
Từ (1) và (2) ⇒ nC2H4 dư = 0,02 ; nC3H6 = 0,03
nC2H4 phản ứng = 0,1 – 0,02 = 0,08
⇒ H = (0,08 : 0,1).100% = 80%
Đáp án B.

Đáp án B
nhh = 0,1 mol.
Giả sư: nC2H4 = nC3H6 = a mol → nH2 = 1 - 2a mol.
→ mX = 28a + 42a + 2(0,1 - 2a) = 15,2 x 0,1
→ a = 0,02 mol.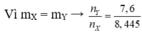
→ nY = 0,09 mol.
Ta có nH2phản ứng = nX - nY = 0,1 - 0,09 = 0,01 mol.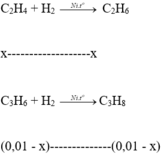
mbình tăng = (0,02 - x) x 28 + (0,02 - 0,01 + x) x 42 = 1,015
→ x = 0,0025 mol.

Đáp án D
Hướng dẫn
nX = 20,16/22,4 = 0,9 mol
nY = 13,44/22,4 = 0,6 mol
nH2 pư = 0,9 – 0,6 = 0,3 mol
nanken dư = 2,8/28 = 0,1 mol
nanken bđ = 0,1 + 0,3 = 0,4 mol
=> nH2 bđ = 0,5 mol
=> H = 0 , 3 0 , 4 .100% = 75%

Đáp án B
0,3375 mol hhX gồm C2H2 và H2 qua Ni, to
→ hhY gồm 3 hiđrocacbon, dY/H2 = 14,25.
MY = 28,5 → hhY có CTC là C2H4,5.
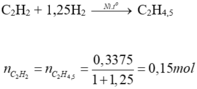
• C2H4,5 + 0,75Br2 → C2H4,5Br1,5
0,15------- 0,1125
→ mBr2 = 0,1125 x 160 = 18 gam

Đáp án C
TQ : CnH2n + H2 -> CnH2n+2
Vì đun nóng trong bình kín nên mX = mY = nX.MX = 1.2.9,25 = 18,5g
=> nY = 0,925 mol
=> nX – nY = nH2 pứ = 1 – 0,925 = 0,075 mol

Đáp án : B
Theo BTKL: mX = 0,04 x 26 + 0,03 x 40 + 0,8 x 2 = 24 gam → nX = 24 : 24 = 1 mol.
Ta có nH2phản ứng = nhh ban đầu - nX = (0,4 + 0,3 + 0,8) - 1 = 0,5 mol.
nπ trước phản ứng = 2 x nCH≡CH + 2 x nCH≡C-CH3 = 2 x 0,4 + 2 x 0,3 = 1,4 mol.
→ nπ dư sau phản ứng = nπ trước phản ứng - nH2 = 1,4 - 0,5 = 0,9.
Mà nπ dư sau phản ứng = 2 x n↓ + nBr2 → n↓ = (0,9 - 0,1) : 2 = 0,4 mol.
Giả sử số mol của AgC≡CAg và AgC≡C-CH3 lần lượt là x, y mol
Ta có hpt: ![]()
→ m = 0,15 x 240 + 0,25 x 147 = 72,75 gam → Chọn C

Đáp án D
hhX gồm H2 và CnH2n có tỉ lệ số mol là 1 : 1.
hhX qua ống đựng Ni, to → hhY có dY/H2 = 23,2. H = b%.
• Coi hh X gồm H2 1 mol; CnH2n - 2 1 mol.
hhY gồm CnH2n + 2 x mol; H2 dư (1 - x) mol và CnH2n (1 - x) mol.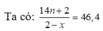
→ 14n + 46,4x = 90,8.
Biện luận → n = 4; x = 0,75 → C4H7; H = 75%

Đáp án A
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni.
Nung bình → hhX có dX/H2 = 8.
Theo BTKL: mhhX = mhh ban đầu = 0,35 x 26 + 0,65 x 2 = 10,4 gam
→ nhhX = 10,4 : 16 = 0,65 mol.
→ nH2phản ứng = nhh ban đầu - nX = 0,35 + 0,65 - 0,65 = 0,35 mol.
Ta có: nπ trước phản ứng = 2 x nCH≡CH = 2 x 0,35 = 0,7 mol.
→ nπ dư = nπ trước phản ứng - nH2 = 0,7 - 0,35 = 0,35 mol.
• Ta có nπ dư = 2 x nAgC≡CAg + nBr2
→ nBr2 = 0,35 - 2 x (12 : 240) = 0,25 mol
Gọi $n_{C_2H_4} = a(mol) ; n_{C_3H_6} = a(mol) ; n_{H_2} = 3a(mol)$
$\Rightarrow 28a + 42a + 3a.2 = 1,52$
$\Rightarrow a = 0,02$
Suy ra : $n_{C_2H_4} = 0,02(mol) ; n_{C_3H_6} = 0,02(mol) ; n_{H_2} = 0,06(mol)$
Do tốc độ phản ứng hidro hoá 2 olefin như nhau nên :
Gọi $n_{C_2H_4\ pư} = 0,02x(mol) ; n_{C_3H_6\ pư} = 0,02x(mol)$
$C_2H_4 + H_2 \xrightarrow{t^o,Ni} C_2H_6$
$C_3H_6 + H_2 \xrightarrow{t^o,Ni} C_3H_8$
Y có :
$n_{C_2H_4\ dư} = 0,02 - 0,02x(mol)$
$n_{C_3H_6\ dư} = 0,02 - 0,02x(mol)$
$C_2H_4 + Br_2 \to C_2H_4Br_2$
$C_3H_6 + Br_2 \to C_3H_6Br_2$
$m_{tăng} = 28(0,02 - 0,02x) + 42(0,02 - 0,02x) = 1,05$
$\Rightarrow x = 0,25$
$n_{H_2\ pư} = 0,02x + 0,02x = 0,04x = 0,01(mol)$
$V_{H_2} = 0,01.22,4 = 0,224(lít)$