Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Fe + 2HCl = FeCl2 + H2
nHCl = 2nFe = 2*5,6/56 = 0,2 mol
=> CMHCl = 0,2/500*1000 = 0,4 M
nH2 = nFe = 5,6/56 = 0,1 mol
=> VH2 = 0,1 * 22,4 = 2,24 lít

nNaHCO3 = 0,4 (mol)
BTNT C, có: nCO2 = nNaHCO3 = 0,4 (mol)
⇒ VCO2 = 0,4.22,4 = 8,96 (l)

giải em vs Đốt cháy hoàn toàn 0.3g hợp chất hữu cơ A thu được 0.224 dm3 khí CO2 ở đktc và 0.18g H2O. Lập công thức của A. vào câu hỏi của e trả lời e vs

Khi cho từ từ hỗn hợp các muối cacbonat trên vào dung dịch HCl thì
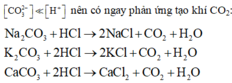
Vì bản chất của phản ứng là phản ứng giữa C O 3 2 - và H+ nên ta có thể đặt công thức chung của các muối và viết phản ứng để dễ quan sát.
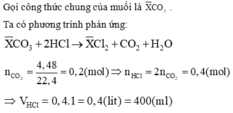
Đáp án D

\(a)2Al + 6CH_3COOH \to 2(CH_3COO)_3Al + 3H_2\\ b)n_{Al} = \dfrac{2,7}{27} = 0,1(mol) ; n_{CH_3COOH} = \dfrac{200.10\%}{60} = \dfrac{1}{3}(mol)\\ n_{CH_3COOH} = \dfrac{1}{3}> 3n_{Al} = 0,3 \to CH_3COOH\ dư\\ n_{H_2} = \dfrac{3}{2}n_{Al} = 0,15(mol) \Rightarrow V_{H_2} = 0,15.22,4 = 3,36(lít)\\ n_{CH_3COOH\ pư} = 3n_{Al} =0,3(mol) \Rightarrow m_{CH_3COOH\ pư} = 0,3.60 = 18(gam)\\ c) m_{dd} = 2,7 + 200 - 0,15.2 = 202,4(gam)\\ n_{(CH_3COO)_3Al} = n_{Al} = 0,1(mol)\\ m_{CH_3COOH\ dư} = 200.10\% - 18 = 2(gam)\\ C\%_{(CH_3COO)_3Al} = \dfrac{0,1.204}{202,4}.100\% = `10,08\%\\ \)
\(C\%_{CH_3COOH} = \dfrac{2}{202,4}.100\% = 0,988\%\)

a) PTHH: CuO + H2SO4 ---> CuSO4 + H2O
b)
n Cu = 1,6 / 80 = 0,02 mol
m H2SO4 = 20 . 100 / 100 = 20 g
=> n H2SO4 = 20 / 98 = 0,204 mol
TPT:
1 mol : 1 mol
0,02 mol : 0,204 mol
=> Tỉ lệ: 0,02/1 < 0,204/1
=> H2SO4 dư, tính toán theo CuO
m dd sau p/ư = m dd H2SO4 + m CuO = 100 + 1,6 = 101,6 g
TPT: n CuSO4 = n CuO = 0,02 mol
=> m CuSO4 = 0,02 . 160 = 3,2 g
=> C% CuSO4 = 3,2 / 101,6 . 100% = 3,15%
n H2SO4 dư = 0,204 - 0,02 = 0,182 mol
=> m H2SO4 dư = 0,182 . 98 =17,836 g
=> C% H2SO4 = 17,836 / 101,6 . 100% = 17,83%
Bạn xem coi có giúp gì được ko nhé!!!

Gọi x, y tương ứng là số mol Mg và MgO: 24x + 40y = 8,8.
x + y = nMgCl2 = 28,5/95 = 0,3
Giải hệ thu được: x = 0,2; y = 0,1.
a) %Mg = 24.0,2/8,8 = 54,54%; %MgO = 100 - 54,54 = 45,46%
b) nHCl = 2(x+y) = 0,6 mol; mdd =36,5.0,6.100/14,6 = 150 gam.
c) mdd sau p.ư = 8,8 + 150 - mH2 = 158,8 - 2.0,2 = 158,4 gam.
%MgCl2 = 28,5/158,4 = 17,99%


nZn = 13/65=0.2 mol
Zn + 2HCl --> ZnCl2 + H2
0.2___0.4______0.2____0.2
VH2 = 0.2*22.4 = 4.48 (l)
Vdd HCl = 0.4/0.5=0.8 (l)
CM ZnCl2 = 0.2/0.8=0.25 M