Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi `n_{Al} = a (mol); n_{Fe} = b (mol)`
PTHH:
`2Al + 3H_2SO_4 -> Al_2(SO_4)_3 + 3H_2`
`Fe + H_2SO_4 -> FeSO_4 + H_`
b) `n_{H_2} = (0,56)/(22,4) = 0,025 (mol)`
Theo PT: `n_{H_2} = n_{Fe} + 3/2 n_{Al}`
`=> b + 1,5a = 0,025`
Giải hpt \(\left\{{}\begin{matrix}27a+56b=0,83\\1,5a+b=0,025\end{matrix}\right.\Leftrightarrow a=b=0,01\)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,01.27}{0,83}.100\%=32,53\%\\\%m_{Fe}=100\%-32,53\%=67,47\%\end{matrix}\right.\)

Đáp án C
Gọi a, b là số mol của Al và Fe trong 8,3 g hỗn hợp ban đầu


PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
\(Cu+2H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}CuSO_4+SO_2\uparrow+2H_2O\)
Ta có: \(n_{SO_2}=\dfrac{0,112}{22,4}=0,005\left(mol\right)=n_{Cu}\)
\(\Rightarrow m_{Cu}=0,005\cdot64=0,32\left(g\right)\) \(\Rightarrow m_{Mg}=10,6-0,32=10,28\left(g\right)\)

2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
x 3/2 x mol
F e + H 2 S O 4 → F e S O 4 + H 2
y y mol
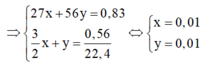
⇒ % m A l = 0,01.27 0,83 .100 = 32,53 % ⇒ % m F e = 100 % − 32,53 % = 67,47 %
⇒ Chọn D.

Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : Zn + H2SO4 → ZnSO4 + H2\(|\)
1 1 1 1
0,1 0,1
Số mol của kẽm
nZn = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Khối lượng của kẽm
mZn = nZn . MZn
= 0,1 . 65
= 6,5 (g)
Khối lượng của đồng
mCu = 10 - 6,5
= 3,5 (g)
0/0Zn = \(\dfrac{m_{Zn}.100}{m_{hh}}=\dfrac{6,5.100}{10}=65\)0/0
0/0Cu = \(\dfrac{m_{Cu}.100}{m_{hh}}=\dfrac{3,5.100}{10}=35\)0/0
Chúc bạn học tốt
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\\ \left(mol\right)....0,1.....0,1...........0,1.....\leftarrow0,1\\ m_{Zn}=0,1.65=6,5\left(g\right)\\ \left\{{}\begin{matrix}\%m_{Zn}=\dfrac{6,5}{10}.100\%=65\%\\\%m_{Cu}=100\%-65\%=35\%\end{matrix}\right.\)

Gọi x, y lần lượt là sô mol của Fe và Mg
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH:
Fe + H2SO4 ---> FeSO4 + H2 (1)
Mg + H2SO4 ---> MgSO4 + H2 (2)
a. Theo PT(1): \(n_{H_2}=n_{Fe}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow x+y=0,3\) (*)
Theo đề, ta có: 56x + 24y = 10.4 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,3\\56x+24y=10,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right);m_{Mg}=0,2.24=4,8\left(g\right)\)
b. Ta có: \(n_{hh}=0,1+0,2=0,3\left(mol\right)\)
Theo PT(1,2): \(n_{H_2SO_4}=n_{hh}=0,3\left(mol\right)\)
Đổi 200ml = 0,2 lít
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,3}{0,2}=1,5M\)

a, PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b, Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow27x+56y=16,6\left(1\right)\)
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Theo PT: \(\Sigma n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{3}{2}x+y\left(mol\right)\)
\(\Rightarrow\dfrac{3}{2}x+y=0,05\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=\\y=\end{matrix}\right.\)
Tới đây ra số mol âm, bạn xem lại đề nhé!

Câu 4 :
Vì bạc không tác dụng với axit sunfuric loãng :
\(n_{H2}=\dfrac{0,224}{22,4}=0,01\left(mol\right)\)
a) Pt : \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2|\)
1 1 1 1
0,01 0,01 0,01
b) \(n_{Zn}=\dfrac{0,0.1}{1}=0,01\left(mol\right)\)
\(m_{Zn}=0,01.65=0,65\left(g\right)\)
\(m_{Ag}=1,73-0,65=1,08\left(g\right)\)
0/0Zn = \(\dfrac{0,65.100}{1,73}=37,57\)0/0
0/0Ag = \(\dfrac{1,08.100}{1,73}=62,43\)0/0
c) \(n_{ZnSO4}=\dfrac{0,01.1}{1}=0,01\left(mol\right)\)
⇒ \(m_{ZnSO4}=0,01.161=1,61\left(g\right)\)
Chúc bạn học tốt
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,15<----------------------0,15
\(m_{Fe}=0,15.56=8,4\left(g\right)\\ \Rightarrow\%m_{Fe}=\dfrac{8,4}{10,5}.100\%=80\%\\ \Rightarrow\%m_{Cu}=100\%-80\%=20\%\)