Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

đặt CT của muối Clorua là \(RCl_n\left(n\inℕ^∗\right)\) là hoá trị của R
PTHH: \(RCl_n+nAgNO_3\rightarrow nAgCl\downarrow+R\left(NO_3\right)_n\)
Theo phương trình \(n_{RCl_n}.n=n_{AgCl}=0,1mol\)
\(\rightarrow\frac{5,35n}{M_R+35,5n}=0,1\)
\(\rightarrow5,35n=0,1M_R+3,55n\)
\(\rightarrow M_R=\frac{1,8}{0,1}n=18n\)
Vậy không có chất R nào thoả mãn.

\(n_M=\dfrac{7,2}{M_M}\left(mol\right)\)
PTHH: M + Cl2 --to--> MCl2
\(\dfrac{7,2}{M_M}\)------------>\(\dfrac{7,2}{M_M}\)
=> \(\dfrac{7,2}{M_M}\left(M_M+71\right)=28,5=>M_M=24\left(Mg\right)\)

a) $Zn + 2HCl \to ZnCl_2 + H_2$
b) Chất phản ứng : $Zn,HCl$
Sản phẩm : $ZnCl_2,H_2$
Tỉ lệ số nguyên tử Zn : Số phân tử $HCl$ là 2 : 1
Tỉ lệ số phân tử $ZnCl_2$ : số phân tử $H_2$ là 1 : 1
c) $m_{Zn} + m_{HCl} = m_{ZnCl_2} + m_{H_2}$
d) $m_{H_2} = 26 + 29,2 - 54,4 = 0,8(gam)$
e) 1 đvC = $\dfrac{1,9926.10^{-23}}{12} = 1,6605.10^{-24}(gam)$
$m_H = 1.1,6605.10^{-24} = 1,6605.10^{-24}(gam)$
$m_{Zn} = 65.1,6605.10^{-24} = 107,9325.10^{-24}(gam)$
f)$n_{H_2} = 0,4(mol) ; n_{CO_2} = \dfrac{0,44}{44} = 0,01(mol)$
$\Rightarrow n_{hh} = 0,4 + 0,01 = 0,41(mol)$
$V_{hh} = 0,41.22,4 = 9,184(lít)$

a) Mg + Cl2 --to--> MgCl2
Tỉ lệ Mg : Cl2 = 1:1
b) Theo ĐLBTKL:
\(m_{Mg}+m_{Cl_2}=m_{MgCl_2}\)
=> \(m_{Cl_2}=19-4,8=14,2\left(g\right)\)
=> \(n_{Cl_2}=\dfrac{14,2}{71}=0,2\left(mol\right)\)
=> \(V_{Cl_2}=0,2.22,4=4,48\left(l\right)\)
c) \(n_{MgCl_2}=\dfrac{3.10^{23}}{6.10^{23}}=0,5\left(mol\right)\)
PTHH: Mg + Cl2 --to--> MgCl2
______0,5<--0,5<--------0,5__________(mol)
=> Số nguyên tử Mg = 0,5.6.1023 = 3.1023
=> Số phân tử Cl2 = 0,5.6.1023 = 3.1023

Gọi KL cần tìm là M
\(n_{AgNO_3}=\dfrac{170}{170}=1(mol)\\ MCl_2+2AgNO_3\to M(NO_3)_2+2AgCl\downarrow\\ \Rightarrow n_{MCl_2}=\dfrac{1}{2}n_{AgNO_3}=0,5(mol)\\ \Rightarrow M_{MCl_2}=\dfrac{55,5}{0,5}=111(g/mol)\\ \Rightarrow M_M=111-35,5.2=40(g/mol)(Ca)\\ n_{Ca(NO_3)_2}=0,5(mol);n_{AgCl}=1(mol)\\ \Rightarrow m_{Ca(NO_3)_2}=0,5.164=82(g);m_{AgCl}=1.143,5=143,5(g)\)

Khi đun nóng :
1g Cu......................................................1,11g Cl
Vậy
64gCu ...................................................71,04g Cl
\(n_{Cu}=\frac{64}{64}=1\left(mol\right)\)
\(n_{Cl}=\frac{71,04}{35,5}=2\left(mol\right)\)
Vậy công thức hoá học của hợp chất là CuCl2

m C l = m A l C l 3 - m A l = 6,675 - 1,35 = 5,325 g
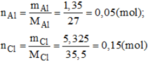
n C l = 3 . n A l ⇒ số nguyên tử Cl gấp 3 số nguyên tử Al. Công thức hóa học đơn giản của nhôm clorua: A l C l 3
BTKL:
\(m_{O_2}=21-1=20\left(g\right)\Rightarrow n_{O_2}=0.625\left(mol\right)\)
\(2Cu+xCl_2\underrightarrow{^{^{t^0}}}2CuCl_x\)
\(2...........x\)
\(\dfrac{1.25}{x}.....0.625\)
\(m_{Cu}=\dfrac{1.25}{x}\cdot64=1\left(g\right)\)
\(\Rightarrow x=80\)
Em xem lại đề nhé !