
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án A
+ Thứ tự phản ứng:
Mg, Fe
AgNO3, Cu(NO3)2
+ Do khi cho dung dịch NaOH dư vào dung dịch E, lọc kết tủa và nung ngoài không khí đến khối lượng không đổi, thu hỗn hợp 2 oxit nên AgNO3 và Cu(NO3)2 phản ứng hết, Mg hết.
Gọi số mol AgNO3 và Cu(NO3)2 lần lượt là x, y.
+ 2 oxit: Fe2O3 và MgO (0,15) => mFe2O3 = 8,4-0,15.40 = 2,4 gam => nFe2O3 = 0,015 mol
=> nFe pư = 0,015.2 = 0,03 mol
+ Khối lượng chất rắn Z: mZ = mFe dư + mAg + mCu => 0,07.56 + 108x + 64y = 20 (1)
+ BT e: 2nMg pư + 2nFe pư = nAg + 2nCu => 2.0,15 + 2.0,03 = x+2y (2)
Giải (1) và (2) => x = 0,06; y = 0,15
Nồng độ AgNO3 và Cu(NO3)2 ban đầu là 0,12M và 0,3M

+ Thứ tự phản ứng:
Mg, Fe
AgNO3, Cu(NO3)2
+ Do khi cho dung dịch NaOH dư vào dung dịch E, lọc kết tủa và nung ngoài không khí đến khối lượng không đổi, thu hỗn hợp 2 oxit nên AgNO3 và Cu(NO3)2 phản ứng hết, Mg hết.
Gọi số mol AgNO3 và Cu(NO3)2 lần lượt là x, y.
+ 2 oxit: Fe2O3 và MgO (0,15) => mFe2O3 = 8,4-0,15.40 = 2,4 gam => nFe2O3 = 0,015 mol
=> nFe pư = 0,015.2 = 0,03 mol
+ Khối lượng chất rắn Z: mZ = mFe dư + mAg + mCu => 0,07.56 + 108x + 64y = 20 (1)
+ BT e: 2nMg pư + 2nFe pư = nAg + 2nCu => 2.0,15 + 2.0,03 = x+2y (2)
Giải (1) và (2) => x = 0,06; y = 0,15
Nồng độ AgNO3 và Cu(NO3)2 ban đầu là 0,12M và 0,3M
Đáp án A

Đáp án A
+ Thứ tự phản ứng:
Mg, Fe
AgNO3, Cu(NO3)2
+ Do khi cho dung dịch NaOH dư vào dung dịch E, lọc kết tủa và nung ngoài không khí đến khối lượng không đổi, thu hỗn hợp 2 oxit nên AgNO3 và Cu(NO3)2 phản ứng hết, Mg hết.
Gọi số mol AgNO3 và Cu(NO3)2 lần lượt là x, y.
+ 2 oxit: Fe2O3 và MgO (0,15) => mFe2O3 = 8,4-0,15.40 = 2,4 gam
=> nFe2O3 = 0,015 mol
=> nFe pư = 0,015.2 = 0,03 mol
+ Khối lượng chất rắn Z: mZ = mFe dư + mAg + mCu
=> 0,07.56 + 108x + 64y = 20 (1)
+ BT e: 2nMg pư + 2nFe pư = nAg + 2nCu => 2.0,15 + 2.0,03 = x+2y (2)
Giải (1) và (2) => x = 0,06; y = 0,15
Nồng độ AgNO3 và Cu(NO3)2 ban đầu là 0,12M và 0,3M

Đáp án B
Có khối lượng chất rắn sau khi nung < mX
=> Chứng tỏ X phản ứng còn dư, Cu(NO3)2 phản ứng hết.
· Trường hợp 1: Mg phản ứng còn dư.
Áp dụng tăng giảm khối lượng có:
nMg phản ứng 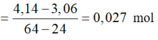
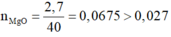 => Vô lý
=> Vô lý
· Trường hợp 2: Fe đã tham gia phản ứng.
Đặt số mol Mg và Fe phản ứng lần lượt là a, b.
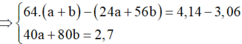
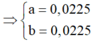
![]()
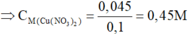

Đáp án B
Ta nhận thấy mE < mX => KL chưa phản ứng hết; AgNO3 và Cu(NO3)2 hết
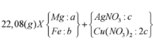
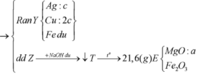
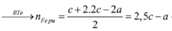
![]()

Đáp án B
Giả sử KOH không dư ⇒ nKNO2 = nKOH = 0,5 mol ⇒ mrắn ≥ mKNO2 = 42,5(g)
⇒ vô lí! ⇒ KOH dư. Đặt nKNO3 = x; nKOH dư = y. Bảo toàn nguyên tố Kali: x + y = 0,5.
Rắn gồm KNO2 và KOH dư ⇒ 85x + 56y = 41,05 ⇒ giải hệ có: x = 0,45 mol; y = 0,05 mol.
Đặt nFe = a; nCu = b ⇒ mA = 56a + 64b = 11,6(g)
16(g) rắn gồm Fe2O3 và CuO.
⇒ 160.0,5a + 80b = 16
⇒ giải hệ có: a = 0,15 mol; b = 0,05 mol.
nHNO3 = 0,7 mol; nNO3–/X = nKNO3 = 0,45 mol. Bảo toàn nguyên tố Nitơ: nN/B = 0,25 mol.
Bảo toàn nguyên tố Hidro: nH2O = 0,35 mol. Bảo toàn nguyên tố Oxi: nO/B = 0,4 mol.
⇒ Bảo toàn khối lượng: mX = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2(g).
-> nNO3–/X < 3nFe + 2nCu ⇒ X gồm muối Fe(NO3)2, Fe(NO3)3 và Cu(NO3)2.
Giải hệ có: nFe(NO3)3 = 0,05 mol
⇒ C%Fe(NO3)3 = 0,05 × 242 ÷ 89,2 × 100% = 13,56%