Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1.
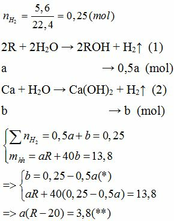
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
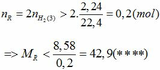
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
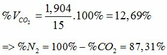
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
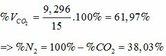

Gọi CTHH của muối là R2CO3
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\n_{BaSO_4}=\dfrac{46,6}{233}=0,2\left(mol\right)\end{matrix}\right.\)
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{BaCO_3}=n_{BaSO_4}=0,2\left(mol\right)=n_{CO_2\left(BaCO_3\right)}\\n_{R_2CO_3}=n_{CO_2\left(còn.lại\right)}=0,3-0.2=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{R_2CO_3}=0,1\cdot\left(2R+60\right)=50-0,2\cdot197=10,6\left(g\right)\)
\(\Rightarrow R=23\)
Vậy kim loại cần tìm là Natri

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

Có: nH2SO4 \(=\frac{4,9}{98}=0,05\left(mol\right)\)
Vì: \(x_1+H2S\text{O4}\rightarrow X_2+X_3\) nên X1 có thể là: oxit bazo, oxit lưỡng tính, bazo, hidroxit lưỡng tính, muối. Nhưng vì bài cho X1 có thể là CaO,MgO,NaOH,KOH,Zn và Fe nên loại các trường hợp oxit lưỡng tính, hidroxit lưỡng tính, muối.
TH1: X1 là oxit bazo: CaO,MgO.
Gọi CTPT chung cho X1 là MgO.
PTPU:
MO + H2SO4 → MSO4 + H2O (*) mol
0,05 0,05 0,05
Vậy KL mol của MO là: \(M_{MO}=\frac{2,8}{0,05}=56\left(g\right)\)
Vậy MO là CaO
TH2: Xét X1 là bazo: NaOH, KOH
Gọi CTPT chung cho X1 là MOH.
PTPƯ: 2MOH + H2SO4 → M2SO4 + 2H2SO4 (**)
0,1 0,05 0,05
Vậy KL mol của MOH là: \(M_{MOH}=\frac{2,8}{0,1}=28\left(g\right)\) (không có MOH thỏa mản)
TH3: X1 kim loại Zn và Fe. Gọi CTCP chung cho X1 là M.
PTPU: M + H2SO4 → MSO4 + H2 (***)
0,05 0,05 0,05
Vậy KL mol MO là \(M_M=\frac{2,8}{0,05}=56\left(g\right)\). Vậy M là Fe.
b. X1 là CaO thì X2 là \(m_{CaS\text{O4}}=0,05.136=6,8\left(g\right)\)
(khác bài ra 7,6 g) loại.
X1 là kim loại Fe thì X2 \(m_{FeS\text{O4}}=0,05.152=7,6\left(g\right)\) phù hợp với đề bài như vậy X3 là H2

Gọi công thức chung 2 muối là ACO3
PTHH: ACO3 + 2HCl --> ACl2 + CO2 + H2O
0,5-------------------->0,5
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,5---->0,5
=> mCaCO3 = 0,5.100 = 50 (g)
=> A
Gọi 2 kim loại đó lần lượt là M và N (II):
PTHH:
MCO3 + 2HCl ---> MCl2 + CO2 + H2O
NCO3 + 2HCl ---> NCl2 + CO2 + H2O
Theo pt: nCO2 = nmuối = 0,5 (mol)
Ca(OH)2 + CO2 ---> CaCO3 + H2O
0,5--------->0,5
=> m = 0,5.100 = 50 (g)
=> A






1.
Gọi kim loại là R \(\rightarrow\) Muối là R2CO3
\(R_2CO_3+2HCl\rightarrow2RCl+CO_2+H_2O\)
Ta có: \(n_{CO2}=\frac{0,224}{22,4}=0,01\left(mol\right)\)
Theo phản ứng: \(n_{R2CO3}=n_{CO2}=0,01\left(mol\right)\)
\(\Rightarrow M_{R2CO3}=2R+60=\frac{1,06}{0,01}=106\Rightarrow R=23\Rightarrow\) R là Na
Vậy Muối là Na2CO3
2.
\(2R+2H_2O\rightarrow2ROH+H_2\)
Ta có: \(n_{H2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow n_R=2n_{H2}=0,15.2=0,3\left(mol\right)\)
\(\Rightarrow M_R=\frac{10,1}{0,3}=33,67\)
Vì 2 kim loại kiềm liên tiếp nhau và 23 < 33,67 < 39 \(\rightarrow\) 2 kim loại là Na và K
Gọi số mol Na là x; K là y
\(\Rightarrow x+y=0,3\left(mol\right)\)
\(\Rightarrow23x+39y=10,1\)
Giải được: \(\rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\rightarrow m_{Na}=0,1.23=2,3\left(g\right)\rightarrow\%m_{Na}=\frac{2,3}{10,1}=22,77\%\)
3.
Ta có:
\(n_{CO2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{Ca\left(OH\right)2}=0,2.1=0,2\left(mol\right)\)
Đặt T = \(\frac{n_{CO2}}{n_{Ca\left(OH\right)2}}=\frac{0,3}{0,2}=1,5\)
\(\Rightarrow1< T< 2\Rightarrow\) Tạo cả hai muối là CaCO3 và Ca(HCO3)2
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
x_________x________________x___________
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
2y___________y_________y_____________
Gọi x, y lần lượt là nCaCO3 và nCa(HCO3)2, ta có:
\(\left\{{}\begin{matrix}x+2y=0,3\\x+y=0,2\end{matrix}\right.\rightarrow x=y=0,1\)
Chất tan trong dd A là Ca(HCO3)2
\(\Rightarrow CM_{Ca\left(HCO3\right)2}=\frac{0,1}{0,2}=0,5M\)
4.
Gọi công thức chung của 2 kim loại kiềm là R
\(2R+2H_2O\rightarrow2ROH+H_2\)
Ta có: \(n_{H2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow_R=2n_{H2}=0,15.2=0,3\left(mol\right)\)
\(\Rightarrow M_R=\frac{10,1}{0,3}=33,67\)
Vì 2 kim loại kiềm liên tiếp nhau và 23 < 33,67 < 39 \(\rightarrow\) 2 kim loại là Na và K
5.
\(2CuO+C\rightarrow2Cu+CO_2\)
Ta có: \(n_{CuO}=\frac{16}{64+16}=0,2\left(mol\right);n_C=\frac{24}{12}=2\left(mol\right)\)
Vì nC > 1/2 nCuO nên C dư
\(\Rightarrow n_{CO2}=\frac{1}{2}n_{CuO}=0,1\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Kết tủa là CaCO3
\(\rightarrow n_{CaCO3}=n_{CO2}=0,1\left(mol\right)\Rightarrow m_{CaCO3}=0,1.100=10\left(g\right)\)
6.
Gọi kim loại là R hóa trị n
\(2R+nCl_2\rightarrow2RCl_n\)
BTKL: mR + mCl2=mRCln
\(\rightarrow m_{Cl2}=11,7-4,6=7,1\left(g\right)\rightarrow n_{Cl2}=\frac{7,1}{35,5.2}=0,1\left(mol\right)\)
\(\Rightarrow n_R=\frac{2n_{Cl2}}{n}=\frac{0,2}{n}\Rightarrow M_R=\frac{46}{\frac{0,2}{n}}=23n\)
Thỏa mãn \(n=1\Rightarrow M_R=23\Rightarrow\) R là Na
7.
X hóa trị IV \(\rightarrow\) Hợp chất với H là XH4
\(\Rightarrow\%m_H=\frac{1.4}{X+1.4}=25\%\Rightarrow X=12\)
Vậy X là C
8.
\(M+2HCl\rightarrow MCl_2+H_2\uparrow\)
\(n_M=\frac{3,6}{M}\)
\(n_{H2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_M=n_{H2}\)
\(\Leftrightarrow\frac{3,6}{M}=0,15\)
\(\Leftrightarrow0,15M=3,6\Leftrightarrow M=24\)
Vậy M là Mg
9.
\(n_{CO2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{NaOH}=0,2.2=0,4\left(mol\right)\)
Ta có :
\(\frac{n_{NaOH}}{n_{CO2}}=\frac{4}{3}\)
\(\Rightarrow\) Tạo ra 2 muối NaHCO3,Na2CO3
\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
a_____2a______________a___________
\(CO_2+NaOH\rightarrow NaHCO_3\)
b______b___________b
Giải hệ phương trình :
\(\left\{{}\begin{matrix}a+b=0,3\\2a+b=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\end{matrix}\right.\)
mmuối=mNa2CO3+mNaHCO3
\(=0,1.106+0,2.84=27,4\left(g\right)\)
10.
\(n_{CO2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CaCO3}=\frac{10}{100}=0,1\left(mol\right)\)
Vì nCaCO3 < nCO2
\(\Rightarrow\) CO2 vẫn còn dư
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\left(1\right)\)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\left(2\right)\)
\(n_{Ca\left(OH\right)2}=n_{CaCO3}=0,1\left(mol\right)\)
\(n_{CO2\left(1\right)}=n_{CaCO3}=0,1\left(mol\right)\)
\(\Rightarrow n_{CO2\left(2\right)}=0,3-0,1=0,2\left(mol\right)\)
\(n_{Ca\left(OH\right)_2\left(2\right)}=\frac{1}{2}n_{CO2}=0,1\left(mol\right)\)
\(n_{Ca\left(OH\right)2}=0,1+0,1=0,2\left(mol\right)\)
\(\Rightarrow V_{Ca\left(OH\right)2}=\frac{0,2}{1}=0,2\left(l\right)=200\left(ml\right)\)
11.
Gọi công thức 2 kim loại là MGọi công thức 2 kim loại là M
Vì là kim loại kiềm thổ nên có hóa trị II
\(M+2HCl\rightarrow MCl_2+H_2\)
\(n_{H2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
\(\Rightarrow n_M=n_{H2}=0,3\left(mol\right)\)
\(\Rightarrow\overline{M_M}=\frac{10,4}{0,3}=34,67\)
Vì M là nhóm kiềm thổVì M là nhóm kiềm thổ
Nên ta có :\(24< \overline{M_M}< 40\)
Vậy hỗn hợp gồm Mg và Ca