Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Định hướng tư duy giải
Ta có:
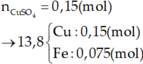
Dễ thấy 6 gam rắn là Fe2O3
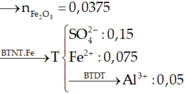
Có Al dư → Phần X phản ứng:
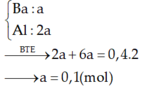
Chú ý: Vì chất tan thu được là Ba(AlO2)2→ tỷ lệ mol Ba : Al phải là 1 : 2
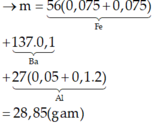

Đáp án B
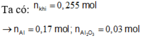
Dung dịch Y chứa 0,23 mol AlCl3.
Cho dung dịch chứa 0,3 mol Ba(OH)2 và 0,37 mol NaOH tác dụng với Y thu được dung dịch Z.
Z chứa Ba2+ 0,3 mol, Na+ 0,37 mol, AlO2- 0,23 mol, OH- dư 0,05 mol.
Cho H2SO4 vào Z.
Để kết tủa Al(OH)3 lớn nhất thì : n H 2 SO 4 = 0 , 23 + 0 , 05 2 = 0 , 14 mol
Để kết tủa BaSO4 lớn nhất thì : n H 2 SO 4
Lúc kết tủa BaSO4 tối đa thì Al(OH)3 bị hòa tan nhưng lượng BaSO4tạo thành lớn hơn Al(OH)3 bị hòa tan nên kết tủa vẫn tăng
→ V = 0 , 3 2 = 0,151 = 150 ml

Đáp án B
Ta có: nNaOH = 0,15 mol; nBa(OH)2 = 0,05 mol
Dung dịch Y chứa 0,15 mol Na+, 0,05 mol Ba2+, u mol AlO2- và v mol OH- dư
Định luật bảo toàn điện tích ta có u + v = 0,15 + 0,05.2 = 0,25 (1)
Ta có: nHCl = 0,32 mol và nH2SO4 = 0,04 mol→ nH+ = 0,4 mol; nSO4(2-) = 0,04 mol
→ nBaSO4 = 0,04 mol
Ta có: mkết tủa = 21,02 gam → nAl(OH)3 = 0,15 mol
Nếu Al(OH)3 chưa bị hòa tan thì nH+ = 0,4 = v + 0,15 (2)
Nếu Al(OH)3 đã bị hòa tan thì nH+ = 0,4 = v + 4u - 3.0,15 (3)
Giải hệ (1) và (2) ra vô nghiệm
Giải hệ (1) và (3) ra u = 0,2 và v = 0,05
Vậy Y gồm Na+ 0,15 mol; 0,05 mol Ba2+; 0,2 mol AlO2- và OH- dư (0,05 mol)
V lít dung dịch Z gồm 0,64V mol HCl và 0,08V mol H2SO4
→ nH+ = 0,8V mol và nSO4(2-) = 0,08 V mol
Khi Al(OH)3 max thì 0,8V = u+ v suy ra V = 0,3125
Suy ra nBaSO4 = 0,025 mol → mkết tủa = 21,425 gam
Khi BaSO4 max thì 0,08V = 0,05 suy ra V = 0,625
Suy ra nH+ = 0,8V = v + 4u-3.nAl(OH)3 → nAl(OH)3 = 7/60 mol → mkết tủa = 20,75 gam
Vậy mkết tủa max = 21,425 gam

Đáp án D
![]()
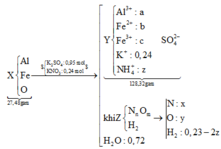
BTKL: mH2O = 27,48 + 0,95.98 + 0,24.101 – 128,32 – 0,2.17,7 = 12,96 gam⇒nH2O = 0,72 mol.
Vì nên Z phải có H2 ⇒ nH2 = 0,95 – 0,72 – 2z = 0,23 – 2z.
Bảo toàn N: x + z = 0,24
Mặt khác, mO.Z = 0,226. 3,54 = 0,8 gam ⇒ nO = y = 0,05 mol
Bảo toàn O: nO.X + 3.0,24 = 0,72 + y ⇔ nO.X = y = 0,05 mol ⇒ coi như oxi không oxh khử.
Khối lượng khí: 14x + 16y + 2. (0,23 – 2z) = 3,54

Bảo toàn điện tích:
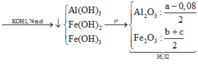
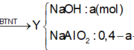
Cho KOH vào Y: OH- phân bổ  còn dư: 0,08 mol hòa tan Al(OH)3
còn dư: 0,08 mol hòa tan Al(OH)3
Vậy nAl(OH)3 = a – 0,08
⇒ hệ 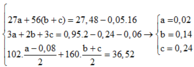
Vậy %mFe(OH)3 =53,90%

Sau phản ứng có Al dư do phản ứng với NaOH tạo H2
=> nAl dư = 2/3 .nH2 = 0,02 mol
Sau phản ứng có Al và Al2O3 + NaOH => NaAlO2
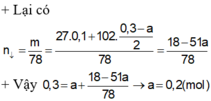
Bảo toàn Al ta có :
2nAl2O3 sau nung= nAl dư + 2nAl2O3 => nAl2O3 = 0,04 mol
=>nAl ban đầu = 0,1 mol
Do các phản ứng hàn toàn , mà khi nhiệt nhôm Al dư => oxit sắt hết
=>D chỉ có Fe
=>Bảo toàn e : 3nFe = 2nSO2 => nFe = 0,08 mol
Bảo toàn khối lượng : mA = mB = mFe + mAl + mAl2O3 = 9,1g
=>%mAl(A) = 29,67% gần nhất với giá trị 24%
=>A

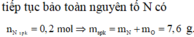

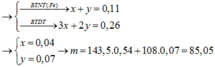


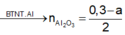
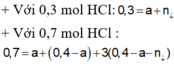
Các phản ứng:
H+ + OH- \(\rightarrow\) H2O (1)
0,04 0,04 mol
Al3+ + 3OH- \(\rightarrow\) Al(OH)3\(\downarrow\)(2)
0,16 0,48 mol 0,16
Theo phương trình (1) và (2) số mol OH- đã phản ứng là: 0,04 + 0,48 = 0,52 mol. Ban đầu tổng số mol OH- là 0,6 mol. Vậy OH- còn dư 0,08 mol.
Do đó một phần Al(OH)3 sẽ bị hòa tan theo phản ứng sau:
Al(OH)3 + OH- \(\rightarrow\) AlO2- + 2H2O (3)
0,16 0,08 mol
Theo phản ứng (3) số mol kết tủa Al(OH)3 còn dư là 0,08 mol. Vậy khối lượng kết tủa thu được là: 78.0,08 = 6,24 gam