Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(1,2H_2+O_2\underrightarrow{t}2H_2O\)
\(2Mg+O_2\underrightarrow{t}2MgO\)
\(2Cu+O_2\underrightarrow{t}2CuO\)
\(S+O_2\underrightarrow{t}SO_2\)
\(4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(C+O_2\underrightarrow{t}CO_2\)
\(4P+5O_2\underrightarrow{t}2P_2O_5\)
\(2,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(a,n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(b,n_C=0,3\left(mol\right)\Rightarrow n_{CO_2}=0,3\left(mol\right)\Rightarrow m_{CO_2}=13,2\left(g\right)\)
c, Vì\(\frac{0,3}{1}>\frac{0,2}{1}\)nên C phản ửng dư, O2 phản ứng hết, Bài toán tính theo O2
\(n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(3,PTHH:CH_4+2O_2\underrightarrow{t}CO_2+2H_2O\)
\(C_2H_2+\frac{5}{2}O_2\underrightarrow{t}2CO_2+H_2O\)
\(C_2H_6O+3O_2\underrightarrow{t}2CO_2+3H_2O\)
\(4,a,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_P=1,5\left(mol\right)\Rightarrow n_{O_2}=1,2\left(mol\right)\Rightarrow m_{O_2}=38,4\left(g\right)\)
\(b,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_C=2,5\left(mol\right)\Rightarrow n_{O_2}=2,5\left(mol\right)\Rightarrow m_{O_2}=80\left(g\right)\)
\(c,PTHH:4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(n_{Al}=2,5\left(mol\right)\Rightarrow n_{O_2}=1,875\left(mol\right)\Rightarrow m_{O_2}=60\left(g\right)\)
\(d,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(TH_1:\left(đktc\right)n_{H_2}=1,5\left(mol\right)\Rightarrow n_{O_2}=0,75\left(mol\right)\Rightarrow m_{O_2}=24\left(g\right)\)
\(TH_2:\left(đkt\right)n_{H_2}=1,4\left(mol\right)\Rightarrow n_{O_2}=0,7\left(mol\right)\Rightarrow m_{O_2}=22,4\left(g\right)\)
\(5,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=0,46875\left(mol\right)\)
\(n_{SO_2}=0,3\left(mol\right)\)
Vì\(0,46875>0,3\left(n_{O_2}>n_{SO_2}\right)\)nên S phản ứng hết, bài toán tính theo S.
\(a,\Rightarrow n_S=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_S=9,6\left(g\right)\)
\(n_{O_2}\left(dư\right)=0,16875\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=5,4\left(g\right)\)
\(6,a,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_C=1,5\left(mol\right)\Rightarrow m_C=18\left(g\right)\)
\(b,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_{H_2}=0,75\left(mol\right)\Rightarrow m_{H_2}=1,5\left(g\right)\)
\(c,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_S=1,5\left(mol\right)\Rightarrow m_S=48\left(g\right)\)
\(d,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_P=1,2\left(mol\right)\Rightarrow m_P=37,2\left(g\right)\)
\(7,n_{O_2}=5\left(mol\right)\Rightarrow V_{O_2}=112\left(l\right)\left(đktc\right)\);\(V_{O_2}=120\left(l\right)\left(đkt\right)\)
\(8,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(m_C=0,96\left(kg\right)\Rightarrow n_C=0,08\left(kmol\right)=80\left(mol\right)\Rightarrow n_{O_2}=80\left(mol\right)\Rightarrow V_{O_2}=1792\left(l\right)\)
\(9,n_p=0,2\left(mol\right);n_{O_2}=0,3\left(mol\right)\)
\(PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
Vì\(\frac{0,2}{4}< \frac{0,3}{5}\)nên P hết O2 dư, bài toán tính theo P.
\(a,n_{O_2}\left(dư\right)=0,05\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=1,6\left(g\right)\)
\(b,n_{P_2O_5}=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=14,2\left(g\right)\)

a.\(n_{CH_4}=\dfrac{V_{CH_4}}{22,4}=\dfrac{6,72}{22,4}=0,3mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,3 0,6 ( mol )
\(V_{O_2}=n_{O_2}.22,4=0,6.22,4=13,44l\)
b.
\(n_P=\dfrac{m_P}{M_P}=\dfrac{3,1}{31}=0,1mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,1 0,05 ( mol )
\(m_{P_2O_5}=n_{P_2O_5}.M_{P_2O_5}=0,05.142=7,1g\)

a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)

a) \(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,4-->0,5------->0,2
=> \(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)
b) \(V_{O_2}=0,5.22,4=11,2\left(l\right)\)
c) Vkk = 11,2.5 = 56 (l)

THAM KHẢO:
Gọi số mol Mg và Zn lần lượt là x, y
Ta có 24x + 65y=23.3
40x + 81y=36.1
=) x=0.7
y= 0.1
b)
c)

\(a,m_C=10.36\%=3,6\left(kg\right)=3600\left(g\right)\\ n_C=\dfrac{3600}{12}=300\left(mol\right)\\ m_S=10-3,6=6,4\left(kg\right)=6400\left(g\right)\\ n_S=\dfrac{6400}{32}=200\left(mol\right)\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ n_{O_2\left(tổng\right)}=n_C+n_S=300+200=500\left(mol\right)\\ V_{O_2\left(tổng\right)\left(đktc\right)}=500.22,4=11200\left(l\right)\\ V_{kk}=\dfrac{100}{20}V_{O_2\left(tổng\right)\left(đktc\right)}=5.11200=56000\left(l\right)\\ b,V_{hh\left(CO_2,SO_2\left(đktc\right)\right)}=22,4.\left(n_C+n_S\right)=22,4.\left(300+200\right)=11200\left(l\right)\)

\(n_C=\dfrac{14,4}{44}=\dfrac{18}{55}\left(mol\right)\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ n_{O_2}=n_C=n_{CO_2}=\dfrac{18}{55}\left(mol\right)\\ a,V_{O_2\left(đktc\right)}=\dfrac{18}{55}.22,4=\dfrac{2016}{275}\left(lít\right)\\ b,V_{kk}=\dfrac{100}{21}.\dfrac{2016}{275}=\dfrac{381}{11}\left(lít\right)\\ c,2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ n_{KClO_3\left(LT\right)}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.\dfrac{18}{55}=\dfrac{12}{55}\left(mol\right)\\ \Rightarrow n_{KClO_3\left(TT\right)}=120\%.\dfrac{12}{55}=\dfrac{72}{275}\left(mol\right)\\ \Rightarrow m_{KClO_3}=122,5.\dfrac{72}{275}=\dfrac{1764}{55}\left(g\right)\)

a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2. Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
VO2 = 2 . 2 = 4 lít.
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
VCO2 = 0,15 . 22,4 = 3,36 lít.
c) Tỉ khối của khí metan và không khí là:
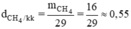
Vậy khí metan nhẹ hơn không khí 0,55.

Câu 2 :
\(n_S=\frac{m_S}{M_S}=\frac{3,2}{32}=0,1\left(mol\right)\)
\(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
- PTHH :........... \(S+O_2\rightarrow SO_2\)
Trước phản ứng:0,1...0,15.......
Trong phản ứng:0,1....0,1......
Sau phản ứng :....0......0,05....
-> Sau phản ứng S phản ứng hết, O2 còn dư ( dư 0,05 mol )
Vậy sau khi đốt cháy trong bình còn khí SO2 và O2 còn dư .
Bài 7 :
PTHH : \(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
\(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
- Theo PTHH : \(n_{KMnO_4}=2n_{O_2}=2.0,1=0,2\left(mol\right)\)
-> \(m_{KMnO_4}=n.M=0,2.158=31,6\left(g\right)\)
Bài 9 :
a, PTHH : \(C+O_2\rightarrow CO_2\)
\(n_{O_2}=\frac{m_{O_2}}{M_{O_2}}=\frac{6,4}{16.2}=0,2\left(mol\right)\)
- Theo PTHH : \(n_{CO_2}=n_{O_2}=0,2\left(mol\right)\)
-> \(m_{CO_2}=n_{CO_2}.M_{CO_2}=0,2.\left(12+16.2\right)=8,8\left(g\right)\)
b, \(n_C=\frac{m_C}{M_C}=\frac{6}{12}=0,5\left(mol\right)\)
\(n_{O_2}=\frac{m_{O_2}}{M_{O_2}}=\frac{20}{32}=0,625\left(mol\right)\)
- PTHH :........... \(C+O_2\rightarrow CO_2\)
Trước phản ứng:0,5..0,625..........
Trong phản ứng:0,5....0,5..........
Sau phản ứng :....0...0,125.......
-> Sau phản ứng C phản ứng hết, O2 còn dư ( dư 0,125 mol )
- Theo PTHH : \(n_{CO_2}=n_C=0,5\left(mol\right)\)
-> \(m_{CO_2}=n_{CO_2}.M_{CO_2}=0,5.\left(12+16.2\right)=22\left(g\right)\)
Bài 12 :
- Đổi : 1 tấn = 1000000 gam .
- Khối lượng than nguyên chất là : \(95\%.1000000=950000\left(g\right)\)
PTHH : \(C+O_2\rightarrow CO_2\)
\(n_C=\frac{m_C}{M_C}=\frac{950000}{12}\approx79167\left(mol\right)\)
- Theo PTHH : \(n_{O_2}=n_C=79167\left(mol\right)\)
-> \(m_{O_2}=n_{O_2}.M_{O_2}=79167.32\approx2533344\left(g\right)\)
-> \(m_{O_2}\approx2,53\) ( tấn )
Vậy cần khoảng 2,53 tấn oxi để đốt cháy hết lượng than trên .
Lần sau nhớ tách câu ra nhé:
1. \(n_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(PTHH:2H_2+O_2\rightarrow2H_2O\)
\(n_{O2}=\frac{n_{H2}}{2}=0,1\left(mol\right)\)
\(\rightarrow V_{O2}=0,1.22,4=2,24\left(l\right)\)
2. \(n_S=\frac{3,2}{32}=0,1\left(mol\right),n_O=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(PTHH:S+O_2\rightarrow SO_2\)
Trước_ 0,1__ 0,15
Phản ứng0,1__0,1
Sau_____0 ___0,05___0,1
Vậy sau phản ứng trong bình có chứa 0,05 mol O2 và 0,1 mol SO2
7. \(n_{O2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Ta có \(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
\(n_{KMnO4}=2n_{O2}=0,2\left(mol\right)\)
\(\rightarrow m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
9.
a. \(n_{O2}=\frac{6,4}{32}=0,2\left(mol\right)\)
\(C+O_2\rightarrow CO_2\)
\(n_{CO2}=n_{O2}=0,2\left(mol\right)\)
\(\rightarrow m_{CO2}=0,2.44=8,8\left(g\right)\)
b. \(n_C=\frac{6}{12}=0,5\left(mol\right),n_{O2}=\frac{20}{32}=0,625\left(mol\right)\)
\(PTHH:C+O_2\rightarrow CO_2\)
Trước ___0,5_0,625___
Phản ứng_0,5 _0,5____
Sau _____0 __ 0,125__0,5
\(\rightarrow m_{CO2}=0,5.44=22\left(g\right)\)
10.
Gọi số mol CO và CO2 là a
\(C+O_2\rightarrow CO_2\)
a___a____ a
\(2C+O_2\rightarrow2CO\)
a___0,5a ____a
Ta có \(n_C=\frac{12}{12}=1\left(mol\right)\)
\(\rightarrow a+a=1\rightarrow a=0,5\left(mol\right)\rightarrow n_{CO2}=a=0,5\left(mol\right)\)
\(\rightarrow V_{CO2}=0,5.22,4=11,2\left(l\right)\)
\(n_{O2}=a+0,5a=1,5a=1,5.0,5=0,75\left(mol\right)\)
\(\rightarrow V_{O2}=0,75.22,4=16,8\left(l\right)\)
11.
Gọi số mol CO và CO2 là a và b
\(PTHH:C+O_2\rightarrow CO_2\)
________a ___ a_____ a
\(2C+O_2\rightarrow2CO\)
b ___0,5b____b
\(n_C=a+b=\frac{12}{12}=1\left(mol\right)\)
Ta có \(M_A=18.2=36\)
\(\rightarrow\frac{44a+28b}{a+b}=36\)
\(\rightarrow44a+28b=36\rightarrow a=b=0,5\)
\(\rightarrow n_{O2}=a+0,5b=0,5+0,5.0,5=0,75\)
\(\rightarrow V_{O2}=0,74.22,4=16,8\left(l\right)\)
\(n_{CO2}=a+b=1\left(mol\right)\)
\(\rightarrow V_{CO2}=1.22,4=22,4\left(l\right)\)
12.
\(PTHH:C+O_2\rightarrow CO_2\)
Đổi: 1 tấn = 1000000 gam
Khối lượng của C trong than là: \(1000000.95\%=950000\left(g\right)\)
Số mol của C là: \(950000:12=79166,67\left(mol\right)\)
Số mol của O2 = \(79166,67\left(mol\right)\)
Khối lượng ôxi cần dùng là: \(79166,67.32=253333,44\left(g\right)\)