Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Cu_2S}=n_{FeS}=a\left(mol\right)\\ 160a+88a=24,8\left(g\right)\\ \rightarrow n_{Cu_2S}=n_{FeS}=0,1\left(mol\right)\)
PTHH:
Cu2S + 6H2SO4 ---> 2CuSO4 + 5SO2 + 6H2O
0,1 ------> 0,6 ----------> 0,2 ------> 0,5 ------> 0,6
2FeS + 10H2SO4 ---> Fe2(SO4)3 + 9SO2 + 10H2O
0,1 ------> 0,5 -----------> 0,05 --------> 0,45 ---> 0,5
\(\rightarrow\left\{{}\begin{matrix}V_{SO_2}=\left(0,5+0,45\right).22,4=21,28\left(l\right)\\n_{H_2SO_4}=0,5+0,6=1,1\left(mol\right)\end{matrix}\right.\)
PTHH:
Fe2(SO4)3 + 6KOH ---> 2Fe(OH)3 + 3K2SO4
0,05 ------------------------> 0,1
CuSO4 + 2KOH ---> Cu(OH)2 + K2SO4
0,2 -----------------------> 0,2
2Fe(OH)3 --to--> Fe2O3 + 3H2O
0,1 ------------------> 0,05
Cu(OH)2 --to--> CuO + H2O
0,2 ----------------> 0,2
\(\rightarrow\left\{{}\begin{matrix}m=107.0,1+98.0,2=20,5\left(g\right)\\a=0,05.160+0,2.80=24\left(g\right)\end{matrix}\right.\)

Các chất tác dụng với H2SO4 đặc nóng tạo khí là: Fe, Fe(OH)2, Fe3O4, Fe(NO3)2, FeSO4, FeCO3.

D sai
Muốn pha loãng axit sunfuric đặc, người ta rót từ từ axit vào nước và khuấy nhẹ bằng đũa thủy tinh mà không làm ngược lại

Do khí amoniac tác dụng với H2SO4 đặc nóng nên không dùng H2SO4 đặc để làm khô khí amoniac, còn khí cacbon và khí oxi không tác dụng nên có thể làm khô được

(1)
Quá trình cho e: \(S^o\rightarrow S^{+4}+4e\)
Quá trình nhận e: \(S^{+6}+2e\rightarrow S^{+4}\) x2
Cân bằng:
\(S+2H_2SO_4\rightarrow3SO_2+2H_2O\)
Tỉ lệ chất khử : chất oxi hóa là 1:2
(2)
Quá trình cho e: \(S^o\rightarrow S^{+4}+4e\)
Quá trình nhận e:\(N^{+5}+e\rightarrow N^{+4}\) x4
Cân bằng:
\(S+4HNO_3\rightarrow4NO_2+2H_2O\)
Tỉ lệ chất khử: chất oxi hóa =1:4
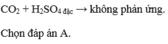
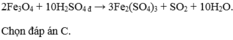
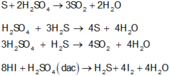

Axit Sunfuric đặc phản ứng với chất nào sau đây (có đun nóng) sinh ra khí SO2?
1, Cu
2, NaOH
3, Al
4, C
5, ZnO
6, HCl
7, HI
Chọn 1,3,4