Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

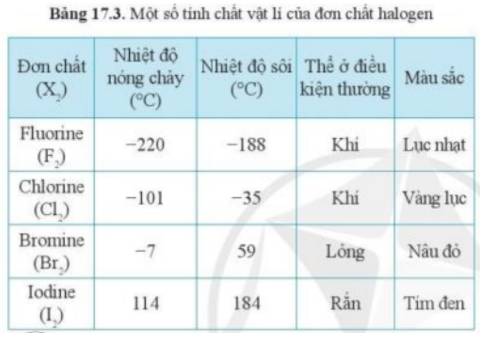
- Theo bảng 17.3, xu hướng biến đổi trạng thái của các halogen ở điều kiện thường từ: khí → lỏng → rắn
- Mà astatine đứng dưới cùng trong nhóm halogen
=> Astatine tồn tại ở thể rắn trong điều kiện thường
- Giải thích: Do sự tăng khối lượng phân tử và sự tăng tương tác van dể Waals

Nguyên tố atatin (Z = 85) thuộc chu kì 6, nhóm VIIA nên có 85e phân bố thành 6 lớp, lớp ngoài cùng có 7e nên thể hiện tính phi kim. At ở cuối nhóm VIIA, nên tính phi kim yếu nhất trong nhóm.

Nguyên tố atatin (Z = 85) thuộc chu kì 6, nhóm VIIA nên có 85e phân bố thành 6 lớp, lớp ngoài cùng có 7e nên thể hiện tính phi kim. At ở cuối nhóm VIIA, nên tính phi kim yếu nhất trong nhóm.

Fr thuộc chu kì 7, đứng cuối nhóm IA. Vì vậy đây là một nguyên tố kim loại, mức độ hoạt động hóa học mạnh (có tính khử mạnh nhất).

So sánh tính chất hóa học của brom với clo và iot.
Brom có tính oxi hóa yếu hơn clo nhưng mạnh hơn iot nên:
Cl2 + 2NaBr → 2NaCl + Br2
Br2 + 2NaI → 2NaBr + I2.

Brom có tính oxi hoầ yếu hơn clo nhưng mạnh hơn iot.
Cl 2 + 2NaBr → 2NaCl + Br 2
Br 2 + 2NaI → 2NaBr + I 2
a) Trong nhóm halogen, đi từ F đến I có độ âm điện giảm dần
=> Tính oxi hóa giảm dần
=> Tính oxi hóa của nguyên tử astatine yếu hơn so với nguyên tử iodine
b) Trong nhóm halogen, đi từ F đến I có màu sắc của các đơn chất đậm dần
=> Đơn chất astatine có màu đậm hơn so với đơn chất iodine