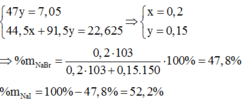Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Cl_2}=0,2\left(mol\right);n_{NaBr}=0,5\left(mol\right);n_{NaI}=0,2\left(mol\right)\)
Cl2 + 2I- ---> I2 + 2Cl-
0,1_____0,2_____________0,2
Cl2 + 2Br- ---> Br2 + 2Cl-
0,1______0,2________________0,2
\(\Rightarrow m_{M'}=m_{NaCl}+m_{NaBr}=54,3\left(g\right)\)

\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\)
\(Cl_2+2NaI\rightarrow2NaCl+I_2\)
Ta có: \(n_{NaCl}=\dfrac{2,8665}{58,5}=0,049\left(mol\right)\)
Theo PT: \(n_{NaCl}=n_{NaBr}+n_{NaI}=0,049\left(mol\right)=x\)
Cho hỗn hợp muối có dạng NaX
PTHH : 2NaX + Cl2 -> 2NaCl + X2
Số mol NaCl \(\dfrac{2,866}{23+35,4}=0,05\left(mol\right)\)
-> molNaX = molNaCl = 0,05 mol

\(n_{Cl_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(n_{NaBr}=0.5\left(mol\right)\)
\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\)
\(0.4..........0.2...........0.4........0.2\)
\(m_X=m_{NaBr\left(dư\right)}+m_{NaCl}=\left(0.5-0.4\right)\cdot103+0.4\cdot58.5=33.7\left(g\right)\)

\(n_{NaBr}=\dfrac{30,9}{103}=0,3\left(mol\right)\)
PTHH: 2NaBr + Cl2 --> 2NaCl + Br2
0,3---------------------->0,15
=> m = 0,15.160 = 24 (g)

\(2NaBr + Cl_2 \to 2NaCl + Br_2\\ 2NaI + Cl_2 \to 2NaCl + I_2\\ n_{Cl_2} =\dfrac{1}{2}n_{NaCl} = \dfrac{1}{2}.\dfrac{23,4}{58,5} = 0,2(mol)\\ \Rightarrow V_{Cl_2} = 0,2.22,4 = 4,48(lít)\)

Đáp án A
Đặt: nNaBr = a(mol), nNaI = b(mol)
Ta có các phản ứng
2NaBr + Cl2→ 2NaCl + Br2(1)
a → a
2NaI + Cl2→ 2NaCl + I2(2)
b → b
Từ (1) và (2) => nNaCl = a+b=1,17/58,5 = 0,02 (mol)
nNaBr + nNaI= a+b = 0,02 (mol)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ: