Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_X=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
- Cho hh khí quá bình 1:
PT: \(C_3H_4+AgNO_3+NH_3\rightarrow AgC_3H_3+NH_4NO_3\)
Ta có: \(n_{AgC_3H_3}=\dfrac{5,88}{147}=0,04\left(mol\right)\)
Theo PT: \(n_{C_3H_4}=n_{AgC_3H_3}=0,04\left(mol\right)\)
- Cho tiếp hh khí còn lại qua bình 2, thấy dd Br2 nhạt màu.
→ Br2 dư, C2H4 pư hết. Khí thoát ra là C3H8.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Ta có: \(n_{C_3H_8}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
a, \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,16-0,08-0,04}{0,16}.100\%=25\%\\\%V_{C_3H_4}=\dfrac{0,04}{0,16}.100\%=25\%\\\%V_{C_3H_8}=50\%\end{matrix}\right.\)
b, Ta có: \(n_X=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
\(\Rightarrow X\left\{{}\begin{matrix}n_{C_2H_4}=0,08.25\%=0,02\left(mol\right)\\n_{C_3H_4}=0,08.25\%=0,02\left(mol\right)\\n_{C_3H_8}=0,04\left(mol\right)\end{matrix}\right.\) \(\Rightarrow n_{\pi}=n_{C_2H_4}+2n_{C_3H_4}=0,06\left(mol\right)\)
\(n_{Br_2}=0,08.1=0,08\left(mol\right)\)
⇒ nπ < nBr2
→ Br2 dư. Hiện tượng: Dd Br2 nhạt màu dần.

\(a)C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ C_3H_4+2Br_2\rightarrow C_3H_4Br_4\\ b)n_{hh}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{Br_2}=0,4.1=0,4\left(mol\right)\\ Đặt:x=n_{C_2H_4};y=n_{C_3H_4}\\ Tacó:\left\{{}\begin{matrix}x+y=0,25\\x+2y=0,4\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\\ \%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,1}{0,25}.100=40\%;\%V_{C_3H_4}=60\%\\ c)X+AgNO_3/NH_3chỉcóC_3H_4pứ\\ C_3H_4+AgNO_3+NH_3\rightarrow C_3H_3Ag+2NH_4NO_3\\ n_{C_3H_2Ag_2}=n_{C_3H_4}=0,15\left(mol\right)\\ \Rightarrow m=0,15.147=22,05\left(g\right)\)

TN1: Gọi \(\left\{{}\begin{matrix}n_{C_3H_6}=a\left(mol\right)\\n_{C_4H_{10}}=b\left(mol\right)\\n_{C_2H_2}=c\left(mol\right)\\n_{H_2}=d\left(mol\right)\end{matrix}\right.\)
nBr2 = 1.0,15 = 0,15 (mol)
Bảo tòan liên kết: a + 2c = d + 0,15
=> a + 2c - d = 0,15
=> 4a + 8c - 4d = 0,6 (3)
TN2: Gọi \(\left\{{}\begin{matrix}n_{C_3H_6}=ak\left(mol\right)\\n_{C_4H_{10}}=bk\left(mol\right)\\n_{C_2H_2}=ck\left(mol\right)\\n_{H_2}=dk\left(mol\right)\end{matrix}\right.\)
=> ak + bk + ck + dk = 0,5 (1)
\(n_{Br_2}=\dfrac{64}{160}=0,4\left(mol\right)\)
Bảo toàn liên kết: ak + 2ck = 0,4 (2)
\(\left(1\right)\left(2\right)\Rightarrow\dfrac{a+b+c+d}{a+2c}=\dfrac{5}{4}\)
=> 4a + 4b + 4c + 4d = 5a + 10c
=> a - 4b + 6c - 4d = 0 (4)
Cần tính: nCO2 = 3a + 4b + 2c (mol)
(3) - (4) => 3a + 4b + 2c = 0,6 - 0 = 0,6
=> nCO2 = 0,6.22,4 = 13,44 (l)
=> C

Đáp án A
(a) Đúng vì ankan chỉ có phản ứng thế Br2.
(b) Sai vì etilen bị oxi hóa khi tác dụng với dung dịch KMnO4. 3C–2H2=C–2H2 + 2KMn+7O4 + 4H2O → 3HO-C–1H2-C–1H2-OH + 2KOH + 2H2O.
(c) Sai vì chỉ có stiren làm mất màu dung dịch thuốc tím ở nhiệt độ thường:
3C6H5-CH=CH2 + 2KMnO4 + 4H2O → 3C6H5-CH(OH)-CH2OH + 2KOH + 2H2O.
(d) Sai vì dung dịch phenol không làm đổi màu quỳ tím.
(e) Sai vì chỉ các ancol đa chức chứa từ 2 -OH kề nhau mới hòa tan được Cu(OH)2.
(g) Đúng: HCHO → AgNO 3 , NH 3 4Ag↓ || HCOOH → AgNO 3 , NH 3 2Ag↓.
⇒ chỉ có (a) và (g) đúng

Ta có:
\(n_{Br2}=0,1.2=0,2\left(mol\right)\)
\(PTHH:C_nH_{2n-2}+2Br_2\rightarrow C_nH_{2n-2}Br_4\)
_________0,1_________0,2___________
\(M_{CnH2n-2}=\frac{4}{0,1}=40\)
\(\Leftrightarrow14n-2=40\)
\(\Leftrightarrow n=3\)
Vậy CTPT của X là C3H4

1. Ta có: \(n_X=0,5\left(mol\right)\)
\(n_{C_3H_4}=n_{AgC_3H_3}=\dfrac{29,4}{147}=0,2\left(mol\right)\)
\(n_{C_3H_6}=n_{Br_2}=0,1.2=0,2\left(mol\right)\)
⇒ nC3H8 = 0,5 - 0,2 - 0,2 = 0,1 (mol)
% số mol cũng là %V ở cùng điều kiện nhiệt độ và áp suất.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_3H_8}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{C_3H_6}=\dfrac{0,2}{0,5}.100\%=40\%\\\%V_{C_3H_4}=40\%\end{matrix}\right.\)
2. Ta có: \(n_{Br_2}=n_{C_3H_6}+2n_{C_3H_4}=0,6\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,6.160=96\left(g\right)\)
\(\Rightarrow m_{ddBr_2}=\dfrac{96}{20\%}=480\left(g\right)\)
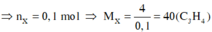
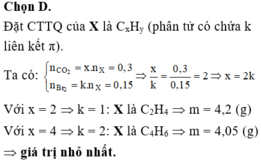
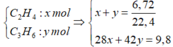

$C_2H_4 + Br_2 \to C_2H_4Br_2$
$n_{Br_2} = n_{C_2H_4} = \dfrac{6,72}{22,4} = 0,3(mol)$
$V_{dd\ Br_2} = \dfrac{0,3}{1} = 0,3(lít) = 300(ml)$