Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: 3Fe + 2O2 → Fe3O4
Số mol của Fe3O4 là: 23,2 : 232 = 0,1 (mol)
Số mol của Fe là: 0,1 . 3 = 0,3 (mol)
Khối lượng Fe nguyên chất tham gia phản ứng là:
0,3 . 56 = 16,8 gam
% tinh khiết của mẩu sắt là: (16,8:21).100% = 80%
Ta có PT:
3Fe + 2O2 ---> Fe3O4
n\(Fe_3O_4\)=\(\frac{23,2}{232}\)=0,1(mol)
Theo PT ta có:
nFe tinh khiết = 3n\(Fe_3O_4\)= 3.0,1=0,3(mol)
mFe tinh khiết = 0,3.56 = 16,8(g)
Độ tinh khiết của sắt đã dùng
= \(\frac{16,8}{21}\).100%=80%

\(1,2H_2+O_2\underrightarrow{t}2H_2O\)
\(2Mg+O_2\underrightarrow{t}2MgO\)
\(2Cu+O_2\underrightarrow{t}2CuO\)
\(S+O_2\underrightarrow{t}SO_2\)
\(4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(C+O_2\underrightarrow{t}CO_2\)
\(4P+5O_2\underrightarrow{t}2P_2O_5\)
\(2,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(a,n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(b,n_C=0,3\left(mol\right)\Rightarrow n_{CO_2}=0,3\left(mol\right)\Rightarrow m_{CO_2}=13,2\left(g\right)\)
c, Vì\(\frac{0,3}{1}>\frac{0,2}{1}\)nên C phản ửng dư, O2 phản ứng hết, Bài toán tính theo O2
\(n_{O_2}=0,2\left(mol\right)\Rightarrow n_{CO_2}=0,2\left(mol\right)\Rightarrow m_{CO_2}=8,8\left(g\right)\)
\(3,PTHH:CH_4+2O_2\underrightarrow{t}CO_2+2H_2O\)
\(C_2H_2+\frac{5}{2}O_2\underrightarrow{t}2CO_2+H_2O\)
\(C_2H_6O+3O_2\underrightarrow{t}2CO_2+3H_2O\)
\(4,a,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_P=1,5\left(mol\right)\Rightarrow n_{O_2}=1,2\left(mol\right)\Rightarrow m_{O_2}=38,4\left(g\right)\)
\(b,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_C=2,5\left(mol\right)\Rightarrow n_{O_2}=2,5\left(mol\right)\Rightarrow m_{O_2}=80\left(g\right)\)
\(c,PTHH:4Al+3O_2\underrightarrow{t}2Al_2O_3\)
\(n_{Al}=2,5\left(mol\right)\Rightarrow n_{O_2}=1,875\left(mol\right)\Rightarrow m_{O_2}=60\left(g\right)\)
\(d,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(TH_1:\left(đktc\right)n_{H_2}=1,5\left(mol\right)\Rightarrow n_{O_2}=0,75\left(mol\right)\Rightarrow m_{O_2}=24\left(g\right)\)
\(TH_2:\left(đkt\right)n_{H_2}=1,4\left(mol\right)\Rightarrow n_{O_2}=0,7\left(mol\right)\Rightarrow m_{O_2}=22,4\left(g\right)\)
\(5,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=0,46875\left(mol\right)\)
\(n_{SO_2}=0,3\left(mol\right)\)
Vì\(0,46875>0,3\left(n_{O_2}>n_{SO_2}\right)\)nên S phản ứng hết, bài toán tính theo S.
\(a,\Rightarrow n_S=n_{SO_2}=0,3\left(mol\right)\Rightarrow m_S=9,6\left(g\right)\)
\(n_{O_2}\left(dư\right)=0,16875\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=5,4\left(g\right)\)
\(6,a,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_C=1,5\left(mol\right)\Rightarrow m_C=18\left(g\right)\)
\(b,PTHH:2H_2+O_2\underrightarrow{t}2H_2O\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_{H_2}=0,75\left(mol\right)\Rightarrow m_{H_2}=1,5\left(g\right)\)
\(c,PTHH:S+O_2\underrightarrow{t}SO_2\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_S=1,5\left(mol\right)\Rightarrow m_S=48\left(g\right)\)
\(d,PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
\(n_{O_2}=1,5\left(mol\right)\Rightarrow n_P=1,2\left(mol\right)\Rightarrow m_P=37,2\left(g\right)\)
\(7,n_{O_2}=5\left(mol\right)\Rightarrow V_{O_2}=112\left(l\right)\left(đktc\right)\);\(V_{O_2}=120\left(l\right)\left(đkt\right)\)
\(8,PTHH:C+O_2\underrightarrow{t}CO_2\)
\(m_C=0,96\left(kg\right)\Rightarrow n_C=0,08\left(kmol\right)=80\left(mol\right)\Rightarrow n_{O_2}=80\left(mol\right)\Rightarrow V_{O_2}=1792\left(l\right)\)
\(9,n_p=0,2\left(mol\right);n_{O_2}=0,3\left(mol\right)\)
\(PTHH:4P+5O_2\underrightarrow{t}2P_2O_5\)
Vì\(\frac{0,2}{4}< \frac{0,3}{5}\)nên P hết O2 dư, bài toán tính theo P.
\(a,n_{O_2}\left(dư\right)=0,05\left(mol\right)\Rightarrow m_{O_2}\left(dư\right)=1,6\left(g\right)\)
\(b,n_{P_2O_5}=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=14,2\left(g\right)\)

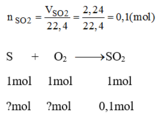
Theo pt: 1 mol S tham gia phản ứng sinh ra 1 mol S O 2
Số mol của lưu huỳnh tham gia phản ứng:
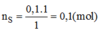
Khối lượng của lưu huỳnh tinh khiết: m S = n S . M S =0,1.32=3,2(g)
Độ tinh khiết của mẫu lưu huỳnh:
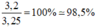

Câu 1)
a) 2HgO\(-t^0\rightarrow2Hg+O_2\)
b)Theo gt: \(n_{HgO}=\frac{2,17}{96}\approx0,023\left(mol\right)\\ \)
theo PTHH : \(n_{O2}=\frac{1}{2}n_{HgO}=\frac{1}{2}\cdot0,023=0,0115\left(mol\right)\\ \Rightarrow m_{O2}=0,0115\cdot32=0,368\left(g\right)\)
c)theo gt:\(n_{HgO}=0,5\left(mol\right)\)
theo PTHH : \(n_{Hg}=n_{HgO}=0,5\left(mol\right)\\ \Rightarrow m_{Hg}=0,5\cdot80=40\left(g\right)\)
Câu 2)
a)PTHH : \(S+O_2-t^0\rightarrow SO_2\)
b)theo gt: \(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
theo PTHH \(n_S=n_{SO2}=0,1\left(mol\right)\\ \Rightarrow m_S=0,1\cdot32=3,2\left(g\right)\)
Ta có khối lượng S tham gia là 3,25 g , khối lượng S phản ứng là 3,2 g
Độ tinh khiết của mẫu lưu huỳnh là \(\frac{3,2}{3,25}\cdot100\%\approx98,4\%\)
c)the PTHH \(n_{O2}=n_{SO2}=0,1\left(mol\right)\Rightarrow m_{O2}=0,1\cdot32=3,2\left(g\right)\)

PTHH: 2xFe + yO2 ==(nhiệt)==> 2FexOy
Áp dụng định luật bảo toàn khối lượng:
=> mO2 = mFexOy - mFe = 3,2 - 2,24 = 0,96 gam
=> nO2 = 0,96 / 32 = 0,03 mol
=> nFe = \(\frac{0,03.2x}{y}=\frac{0,06x}{y}\)
=> mFe = \(\frac{0,06x}{y}.56=2,24\)
=> \(\frac{x}{y}=\frac{2}{3}\)
=> Công thức hóa học: Fe2O3
nFe=0.04 mol
2xFe + yO2 -> 2FexOy
2x : y: 2
=>nFexOy=nFe/x=0.04/x mol
NFexOy=3,2:(56x+16y)
=>0.04/x=3.2/(56x+16y)
<=>25x=(56x+16y):3.2
<=>25x=17.5x+5y
<=>7.5x=5y
<=>x/y=2/3
<=>Fe2O3

PTHH: 2xFe + yO2 ==(nhiệt)==> 2FexOy
Áp dụng định luật bảo toàn khối lượng:
=> mO2 = mFexOy - mFe = 3,2 - 2,24 = 0,96 gam
=> nO2 = 0,96 / 32 = 0,03 mol
=> nFe = \(\frac{0,03.2x}{y}=\frac{0,06x}{y}\)
=> mFe = \(\frac{0,06x}{y}.56=2,24\)
=> \(\frac{x}{y}=\frac{2}{3}\)
=> Công thức hóa học: Fe2O3
nFe=0.04 mol
2xFe + yO2 -> 2FexOy
2x : y: 2
=>nFexOy=nFe/x=0.04/x mol
NFexOy=3,2:(56x+16y)
=>0.04/x=3.2/(56x+16y)
<=>25x=(56x+16y):3.2
<=>25x=17.5x+5y
<=>7.5x=5y
<=>x/y=2/3
<=>Fe2O3

\(PTHH:3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ BTKL:m_{O_2}=m_{Fe_3O_4}-m_{Fe}=23,2-16,8=6,4(g)\)
13) \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(n_{Fe_3O_4}=\frac{23,2}{232}=0,1mol\)
\(n_{Fe}=3.n_{Fe_3O_4}=3.0,1=0,3mol\)
\(m_{Fe\left(tinhkhiết\right)}=0,3.56=16,8g\)
Độ tinh khiết là: \(\frac{16,8}{21}.100\left(\%\right)=80\%\)
16) a) S+O2=to=>SO2
\(n_{O_2}=n_{SO_2}=1,5mol\)
b) S+O2=to=>SO2
\(n_S=\frac{38,4}{32}=1,2mol\)
\(n_{SO_2}=n_S=1,2mol\)