4,95 : y = 0,86 (dư 0,048)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



thương của phép chia 235 : 17,2 là 13,66 số dư là 0,048
bạn tk mik nha

65,73 x 0,86 + 43,27 x 0,86
= 0,86 x (65,73 + 43,27)
= 0,86 x 109
= 0,86 x 100 + 0,86 x 10 - 0,86
= 86 + 8,6 - 0,86
= 94,6 - 0,86 = 93,74
65,73 x 0,86 + 43,27 x 0,86
=0,86*(65,73+43,27)
=0,86*109
=0,86*(100+9)
=0,86*100+0,86*9
=86+7,74
=93,74

a) 32 : 2.4 =13.33333333 đề bài yêu cầu là có 2 c/s ở PTP nên ta lấy 2 c/s ở PTP vậy 32:2.4=13.33
b)4.95 :5.7=0.86842......... đề bài yêu cầu có 2 c/s ở PTP nên ta lấy 2 c/s ở PTP vậy 4.95:5.7=0.86

Giải:
a) \(B=2x\left(y-z\right)+\left(z-y\right)\left(x+m\right)\)
\(\Leftrightarrow B=\left(z-y\right)\left(x+m\right)-2x\left(z-y\right)\)
\(\Leftrightarrow B=\left(z-y\right)\left(x+m-2x\right)\)
\(\Leftrightarrow B=\left(z-y\right)\left(m-x\right)\)
Thay các giá trị của biến vào, ta được:
\(B=\left(10,6-24,6\right)\left(-31,7-18,3\right)\)
\(\Leftrightarrow B=\left(-14\right)\left(-50\right)=700\)
b) \(C=\left(x-y\right)\left(y+z\right)+y\left(y-x\right)\)
\(\Leftrightarrow C=\left(x-y\right)\left(y+z\right)-y\left(x-y\right)\)
\(\Leftrightarrow C=\left(x-y\right)\left(y+z-y\right)\)
\(\Leftrightarrow C=\left(x-y\right)z\)
Thay các giá trị của biến vào, ta được:
\(C=\left(0,86-0,26\right).1,5\)
\(\Leftrightarrow C=1,12.1,5=1,68\)
Vậy ...

Đáp án B
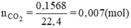
BT nguyên tố ⇒ nC = nCO2 = 0,007 mol
Khối lượng C là mC = 12. 0,007 = 0,084 (g)
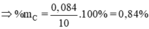

a) \(C_2H_4 + Br_2 \to C_2H_4Br_2\)
b)
\(n_{C_2H_4} = n_{Br_2} = \dfrac{5,6}{160} = 0,035(mol)\\ \%V_{C_2H_4} = \dfrac{0,035.22,4}{0,86}.100\% = 91,16\%\\ \%V_{CH_4} = 100\% - 91,16\% = 8,84\%\)

- Cho 4,95 (g) R pư với HCl, thấy kim loại dư.
Ta có: \(n_{HCl}=\dfrac{5,475}{36,5}=0,15\left(mol\right)\)
PT: \(R+2HCl\rightarrow RCl_2+H_2\)
\(n_{R\left(pư\right)}=\dfrac{1}{2}n_{HCl}=0,075\left(mol\right)\)
\(n_{R\left(banđau\right)}>0,075\Rightarrow\dfrac{4,95}{M_R}>0,075\Rightarrow M_R< 66\left(g/mol\right)\) (1)
- Cho 18,6 (g) hh Fe và R pư với H2SO4 dư.
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{hh}=n_{Fe}+n_R=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow\overline{M_{hh}}=\dfrac{18,6}{0,3}=62\left(g/mol\right)\)
Mà: MFe < 62 (g/mol) → MR > 62 (g/mol) (2)
Từ (1) và (2) ⇒ 62 < MR < 66
→ R là Zn (65 g/mol)
4,95 : y = 0,86 (dư 0,048)
=>4,95=0,86.y+0,048
0,86.y=4,95-0,048
0,86.y=4,902
y=4,902;0,86
y=5,7