trộn lẫn 150 gam dung dịch k2co3 10% với 45 gam k2co3.xH2O thu được dung dịch k2co3 15%. tìm x
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


K2CO3 + H2SO4 --> K2SO4 + CO2 + H2O
x(mol) x(mol) 44x(g)
Gọi x(mol) là số mol K2CO3
Khối lượng dung dịch sau phản ứng: 150 + 200 -44x = 350 - 44x
Ta có: 174x/(350 - 44x)= 10,2: 100= 0,102
Giải ta được: x = 0,2
Còn lại tao nghĩ mày tự giải được

200ml = 0,2l
\(n_{K2CO3}=1.0,2=0,2\left(mol\right)\)
Pt : \(Ca\left(OH\right)_2+K_2CO_3\rightarrow CaCO_3+2KOH|\)
1 1 1 2
0,2 0,2
\(n_{CaCO3}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{CaCO3}=0,2.100=20\left(g\right)\)
⇒ Chọn câu : B
Chúc bạn học tốt
Chọn B.
\(n_{K_2CO_3}=0,2\cdot1=0,2mol\)
\(Ca\left(OH\right)_2+K_2CO_3\rightarrow CaCO_3+2KOH\)
0,2 0,2
\(m_{CaCO_3}=0,2\cdot100=20\left(g\right)\)

a/ A+ HCl
CO3 2- + 2H+ ---> H2O+ CO2
dd B trung hòa bởi NaOH--> trong B có Ba(HCO3)2
CO2 + Ba(OH)2 --> BaCO3 + H2O
0.2<---0.25-0.05-------->0.2
2Co2+ Ba(OH)2--> Ba(HCO3)2
0.1<--------0.05<---------0.05
Ba(HCO3)2+ 2NaOH---> BaCO3+ Na2CO3+ 2H2O
0.05<-------------0.1
--> m2= 0.2*197=39,4g
Na2CO3 va K2CO3 : x,y mol
x+y=0.3
138y=106x*2,604
-->x=0.1,y=0.2
--> m1=0.1*106+ 0,2*138=38,2
b/
C%Na2CO3= (0.1*106*100)/ (61,8+ 38,2)=10,6%
C%K2CO3=(0.2*138*100)/(61,8+ 38,2)=27,6%

Đáp án B
![]()
Như vậy, trong X chỉ có 0,2 mol CO3 2-
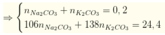
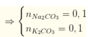
=> Đáp án B

SK2CO3 ở 15oC = mK2CO3 / mdung dịch . 100
=> 21 = mK2CO3 / 24,2 . 100
=> mK2CO3 = 5,082
Mà mdung dịch = mK2CO3 + mH2O
=> 24,2 = 5,082 + mH2O
=> mH2O = 19,118g
Vậy ở 15oC hòa tan 5,082g K2CO3 và 19,118g H2O để thu được 24,2g dung dịch bão hòa .


mdd = 150 + 45 = 195 gam
Trong 195 gam dd \(K_2CO_3\) 15% có chứa \(m_{K_2CO_3}\) = 29,25 gam
Trong 150 gam dd\(K_2CO_3\) 10% có m \(K_2CO_3\) = 15 gam
=> m \(K_2CO_3\) trong 45 gam \(K_2CO_3.xH_2O\) là 29,25 - 15 =14,25 gam ; n \(K_2CO_3.xH_2O\) = n \(K_2CO_3\)(trong muối kết tinh) = 14,25/74,5 = 0,19 mol
=> m \(H_2O\) = 45 - 14,25 = 30,75 gam => n \(H_2O\)(trong kết tinh) = 1,7 mol
\(x=\dfrac{n_{H_2O}}{n}\)=9
=> \(K_2CO_3.9H_2O\)