nguyên tố x có tổng số hạt (p,n,e) là 58 trong đó tổng số hạt mang điện trong nguyên tử gấp 1,9 lần số hạt không mang điện. Số hạt p,n,e của X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a. Ta có: p + e + n = 40
Mà p = e, nên: 2p + n = 40 (1)
Theo đề, ta có: 2p - n = 12 (2)
Từ (1) và (2), ta có HPT:
\(\left\{{}\begin{matrix}2p+n=40\\2p-n=12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=28\\2p-n=12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=14\\p=13\end{matrix}\right.\)
Vậy p = e = 13 hạt, n = 14 hạt.
Dựa vào bảng hóa trị, suy ra:
X là nhôm (Al)
b. Bn dựa vào câu a mik làm rồi làm tiếp câu b nhé.

tham khảo:
Cho nguyên tử X có tổng số hạt p,n,e là 34→2p+n=34
Hạt mang điện nhiều hơn hạt không mang điện là 12
→2p-n=12
Giải hệ ta được
p=e=11,5
n=11

Tổng số hạt trong nguyên tử X là 52:
\(2p+n=52\left(1\right)\)
Số hạt không mang điện lớn hơn số hạt mang điện trong hạt nhân là 1
\(n-p=1\)
\(\Leftrightarrow-p+n=1\left(2\right)\)
\(\left(1\right),\left(2\right):p=e=17,n=18\)
\(X:Cl\left(Clo\right)\)
Gọi số proton, notron,electron lần lượt là p,n,e
Theo bài ta có:
\(p+n+e=52\)
\(\Leftrightarrow3p+n=52\left(p=e\right)\left(1\right)\)
Mặt khác: \(n-p=1\left(2\right)\)
Từ 1 và 2 suy ra \(\left\{{}\begin{matrix}2p+n=52\\n-p=1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=17\\n=18\end{matrix}\right.\)
=>X là Clo. Kí hiệu: Cl

1/ta có hệ: \(\begin{cases}2p+n=36\\2p=12\end{cases}\)
<=> p=e=6
n=24
2) ta có hệ : \(\begin{cases}2p+n=52\\n-p=1\end{cases}\)=> p=e=17 , n=18
=> X là Clo (Cl)

cái 17+ là của clo nha
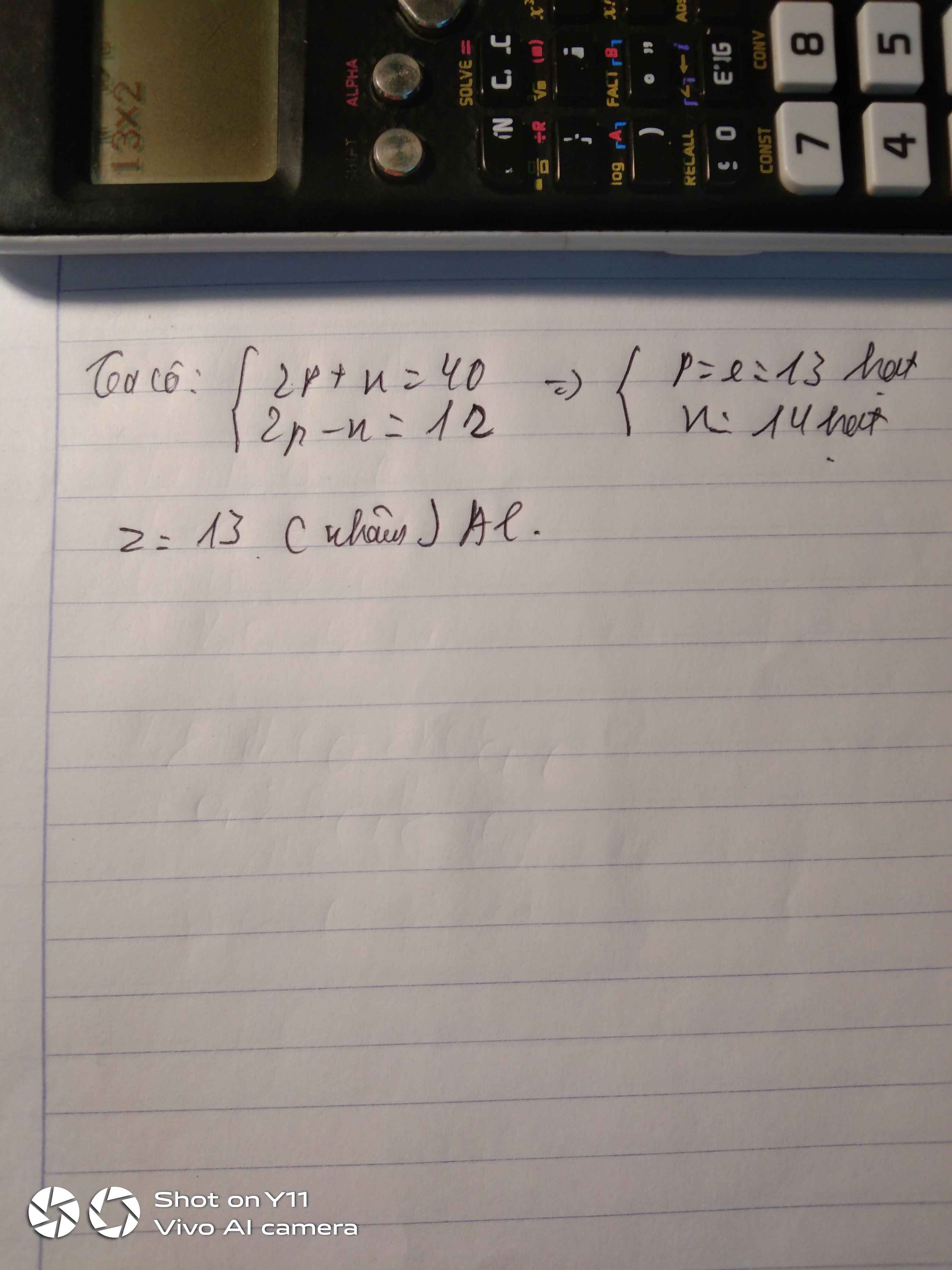
Ta có: P + N + E = 58
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 58 (1)
- Trong đó tổng số hạt mang điện gấp 1,9 lần số hạt không mang điện.
⇒ 2P = 1,9N (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=19\\N=20\end{matrix}\right.\)