Cho 1,2395g Fe tác dụng hết với dung dịch axit clohiđric (HCl) tạo ra m gam muối sắt (II) clorua FeCl2 và V lít khí hiddro H2
a) Khối lượng axit HCL đã tham gia phản ứng là
b) Tính khối lượng muối thu được
c) Tính giá trị của V ở đkc
em cần gấpp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,\text{Sơ đồ p/ứ: }Fe+HCl\to FeCl_2+H_2\\ b,PTHH:Fe+2HCl\to FeCl_2+H_2\\ c,\text{Bảo toàn KL: }m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\\ \Rightarrow m_{HCl}+56=150+8=158\\ \Rightarrow m_{HCl}=102(g)\)

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ a,PTHH:Fe+2HCl\to FeCl_2+H_2\\ b,n_{HCl}=2n_{H_2}=0,3(mol);n_{FeCl_2}=n_{H_2}=0,15(mol)\\ \Rightarrow m_{HCl}=0,3.36,5=10,95(g)\\ m_{FeCl_2}=0,15.127=19,05(g)\)

Gọi \(n_{Fe}=x\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{FeCl_2}=n_{Fe}=x\left(mol\right)\)
Vì khối lượng muối FeCl2 tăng 7,1g so với khối lượng bột Fe
\(\Rightarrow127x-56x=7,1\\ \Rightarrow x=0,1\)
\(n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ V_{H_2\left(ĐKTC\right)}=0,1.22,4=2,24\left(l\right)\)
Chọn D

a) \(PTHH:Fe+HCL\) → \(FeCl_2+H_2\)
Cân bằng: \(Fe+2HCl\) → \(FeCl_2+H_2\)
b) \(n_{Fe}=\dfrac{m}{M}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_{HCl}=2.n_{Fe}=2.0,1=0,2\left(mol\right)\)
\(m_{HCl}=n.M=0,2.36,5=7,3\left(g\right)\)
c) \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(V_{H_2\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)

`a)`
PTHH : `Fe + 2HCl -> FeCl_2 + H_2`
`b)`
`n_{Fe} = (11,2)/(56) = 0,2` `mol`
`n_{HCl} = 2 . n_{Fe} = 0,4` `mol`
`m_{HCl} = 0,4 . 36,5 = 14,6` `gam`
`c)`
`n_{FeCl_2} = n_{Fe} = 0,2` `mol`
`m_{FeCl_2} = 0,2 . 127 = 25,4` `gam`
`n_{H_2} = n_{Fe} = 0,2` `mol`
`V_{H_2} = 0,2 . 22,4 = 4,48` `l`

a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b+c) Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)=n_{FeCl_2}=n_{H_2}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{FeCl_2}=0,2\cdot127=25,4\left(g\right)\\V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\end{matrix}\right.\)
d) Số phân tử H2: \(0,2\cdot6\cdot10^{23}=1,2\cdot10^{23}\left(phân.tử\right)\)
e)
+) Cách 1: Theo PTHH: \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\) \(\Rightarrow m_{HCl}=0,4\cdot36,5=14,6\left(g\right)\)
+) Cách 2:
Ta có: \(m_{H_2}=0,2\cdot2=0,4\left(g\right)\)
Bảo toàn khối lượng: \(m_{HCl}=m_{FeCl_2}+m_{H_2}-m_{Fe}=14,6\left(g\right)\)

\(a.Fe+2HCl\rightarrow FeCl_2+H_2\\b.n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ \Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\\ c.n_{FeCl_2}=n_{Fe}=0,1\left(mol\right)\\ m_{FeCl_2}=0,1.127=12,7\left(g\right) \)

BTKL: \(m_{Fe}+m_{HCl}=m_{muối}+m_{H_2}\)
\(\Rightarrow m_{H_2}=5,6+7,3-12,7=0,2\left(g\right)\)
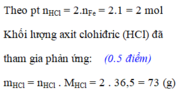
\(n_{Fe}=\dfrac{1,2395}{56}=0,022\left(mol\right)\)
a)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,022 0,044 0,022 0,022
\(m_{HCl}=0,044.36,5=1,606\left(g\right)\)
b)
\(m_{FeCl_2}=0,022.127=2,794\left(g\right)\)
c) \(V_{H_2}=0,022.24,79=0,54538\left(l\right)\)