Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(n_{Fe}=x\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{FeCl_2}=n_{Fe}=x\left(mol\right)\)
Vì khối lượng muối FeCl2 tăng 7,1g so với khối lượng bột Fe
\(\Rightarrow127x-56x=7,1\\ \Rightarrow x=0,1\)
\(n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ V_{H_2\left(ĐKTC\right)}=0,1.22,4=2,24\left(l\right)\)
Chọn D

a) nFe=0,1(mol); nHCl=0,4(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
Ta có: 0,1/1 < 0,4/2
=> Fe hết, HCl dư, tish theo nFe.
b) nH2=nFeCl2=Fe=0,1(mol)
=> V(H2,đktc)=0,1.22,4=2,24(l)
c) mFeCl2=127.0,1=12,7(g)
a) nFe=0,1(mol); nHCl=0,4(mol) PTHH: Fe + 2 HCl -> FeCl2 + H2 Ta có: 0,1/1 < 0,4/2 => Fe hết, HCl dư, tish theo nFe. b) nH2=nFeCl2=Fe=0,1(mol) => V(H2,đktc)=0,1.22,4=2,24(l) c) mFeCl2=127.0,1=12,7(g)

\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 < 0,4 ( mol )
0,1 0,1 ( mol )
\(V_{H_2}=0,1.22,4=2,24l\)
\(n_{ZnCl_2}=\dfrac{0,1.1}{1}=0,1mol\)

Chổ này H2 phải là 0.2 (g) nhé !
Áp dụng định luật bảo toàn khối lượng :
\(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(m_{HCl}=12.7+0.2-5.6=7.3\left(g\right)\)
- Theo ĐLBTKL: \(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
=> \(m_{HCl}=12,7+0,2-5,6=7,3\left(g\right)\)
Check lại đề chứ 0,1 mol Fe pư s ra đc 1 mol H2 :D

BTKL: \(n_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(\Rightarrow m_{HCl}=12,7+0,2-5,6=7,3(g)\)
Chọn B

\(a,\text{Sơ đồ p/ứ: }Fe+HCl\to FeCl_2+H_2\\ b,PTHH:Fe+2HCl\to FeCl_2+H_2\\ c,\text{Bảo toàn KL: }m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\\ \Rightarrow m_{HCl}+56=150+8=158\\ \Rightarrow m_{HCl}=102(g)\)

`a)PTHH:`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,3` `0,6` `0,3` `0,3` `(mol)`
`n_[Fe]=[22,4]/56=0,4(mol)`
`n_[HCl]=0,3.2=0,6(mol)`
Ta có:`[0,4]/1 > [0,6]/2`
`=>Fe` dư
`b)m_[FeCl_2]=0,3.127=38,1(g)`
`c)m_[Fe(dư)]=(0,4-0,3).56=5,6(g)`
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(n_{HCl}=0,3.2=0,6\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Xét: \(\dfrac{0,4}{1}>\dfrac{0,6}{2}\) ( mol )
0,3 0,6 0,3 ( mol )
\(m_{FeCl_2}=0,3.127=38,1\left(g\right)\)
\(m_{Fe\left(dư\right)}=\left(0,4-0,3\right).56=5,6\left(g\right)\)


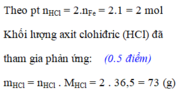

BTKL: \(m_{Fe}+m_{HCl}=m_{muối}+m_{H_2}\)
\(\Rightarrow m_{H_2}=5,6+7,3-12,7=0,2\left(g\right)\)