Một trong những ứng dụng của axetilen là làm nhiên liệu trong đnè xì để hàn và cắt kim loại. Hãy giải thích vì sao người ta ko dùng etan(C2H6) thay cho axetilen, mặ dù nhiệt đốt cháy ở cùng điều kiện của etan (1562kJ/mol) cao hơn của axetilen (1302kJ/mol)
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

23 tháng 4 2023
\(n_{C_2H_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
PT: \(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{5}{2}n_{C_2H_2}=5\left(mol\right)\)
\(\Rightarrow V_{O_2}=5.22,4=112\left(l\right)\)

15 tháng 8 2017
Chọn C.
Axetilen là một ankin có công thức phân tử là C2H2.

15 tháng 8 2017
Đáp án C
Axetilen là một ankin có công thức phân tử là C2H2.

6 tháng 9 2019
Đáp án C
Axetilen là một ankin có công thức phân tử là C2H2.

21 tháng 6 2018
Đáp án C
Axetilen là một ankin có công thức phân tử là C2H2
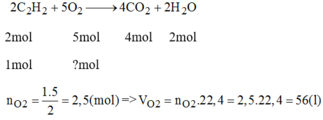
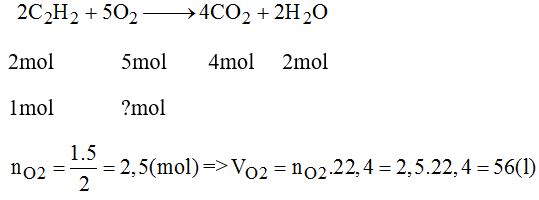



PTHH: \(C_2H_2+\dfrac{5}{2}O_2\xrightarrow[]{t^o}2CO_2+H_2O\)
\(C_2H_6+\dfrac{7}{2}O_2\xrightarrow[]{t^o}2CO_2+3H_2O\)
Ta thấy khi đốt axetilen, lượng nước giải phóng ra ít hơn so với đốt etan. Vì vậy lượng nước thoát ra làm nguội cũng ít hơn. Do đó đốt axetilen nhiệt độ cao hơn
PTHH :
`C_2H_2 + 5/2O_2` `->^{t^o} CO_2 + H_2O`
`C_2H_6 + 7/2O_2 ->^{t^o} CO_2 + 3H_2O`
Dựa vào PTHH ta thấy được lượng nước giải phóng của etan nhiều hơn của axetilen. Nên khi đốt axetilen có nhiệt độ cao hơn giúp cắt kim loại và làm đèn xì tốt hơn.