Methane là một nguyên liệu sạch , thân thiện với môi trường.Xét phản ứng đốt cháy methane trong buồng đốt động cơ xe buýt sử dụng nguyên liệu CNG Tính thể tích khí co2 (điều kiện chuẩn) ở 25°C, 1bar từ 24,79 lít khí CH4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(PTHH:CH_4+2O_2-^{t^o}>CO_2+2H_2O\)
tỉ lệ 1 ; 2 : 1 ; 2
n(mol) 0,1------->0,2------>0,1------->0,2
\(V_{CO_2\left(dkc\right)}=n\cdot24,79=0,1\cdot24,79=2,479\left(l\right)\\ m_{H_2O}=n\cdot M=0,2\cdot18=3,6\left(g\right)\)

\(n_{CH_4}=\dfrac{V}{22,4}=\dfrac{11,2}{22,4}=0,5mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,5 1 0,5 ( mol )
\(V_{O_2}=n.24,79=1.24,79=24,79l\)
\(V_{CO_2}=n.24,79=0,5.24,79=12,395l\)
nCH4 = 11,2/22,4 = 0,5 (mol)
PTHH: CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: 0,5 ---> 1
VO2 = 1 . 24,79 = 24,79 (l)


Do lấy dư 20% oxi so với lượng cần đốt cháy nên lượng oxi đã lấy là:


Tổng khối lượng CO2 và SO2 :
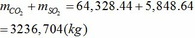
Chú ý:
Lượng O2 lấy dư 20% so với với lượng cần thiết => tính mol O2 chính xác

CH4+2O2-to>CO2+2H2O
0,2-----0,4------0,2
n CH4=0,2 mol
=>mCO2=0,2.44=8,8g
=>VO2=0,4.22,4=8,96l
=>Vkk=8,96.5=44,8l
nCH4 = 4,48:22,4 = 0,2 (mol)
pthh : CH4 + 2O2 -t-> CO2 + 2H2O
0,2 0,4 0,2
mCO2 = 0,2 . 44 = 8,8 (G)
VO2 = 0,4 . 22,4 = 8,96 (L)
=> Vkk = VO2 : 20% = 8,96 : 20% = 44,8 (L)

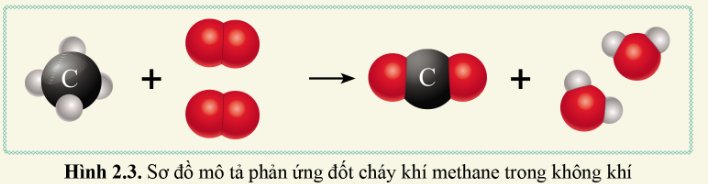
a. Trước phản ứng, có các chất là C, H, O.
- Những nguyên tử H đã liên kết với nguyên tử C, nguyên tử O liên kết với nguyên tử O.
b. Sau phản ứng, có các chất được tào thành là CO2, H2O.
- Những nguyên tử O đã liên kết với nguyên tử C, những nguyên tử H đã liên kết với những nguyên tử O.
c. Số nguyên tử C, H, O trước phản ứng và sau phản ứng đều bằng nhau

\(\Delta_fH^{^{ }o}_{298}\left[CH_4\right]=-\left(-890,3-\left(-393,5\right)-\left(-285,8\right)\right)\\ \Delta_fH^{^{ }o}_{298}\left[CH_4\right]=211kJ\cdot mol^{-1}\)

Chọn C
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nO2 = 0,625 mol
=> nkk = 5nO2 = = 3,125 mol => Vkk = 70 lit

\(n_{CH_4}=\dfrac{24,79}{24,79}=1\left(mol\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(n_{CO_2}=n_{CH_4}=1\left(mol\right)\Rightarrow V_{CO_2}=1.24,79=24,79\left(l\right)\)
\(n_{CH_4}=\dfrac{24,79}{24,79}=1mol\\ CH_4+2O_2\xrightarrow[]{t^0}CO_2+2H_2O\\ n_{CO_2}=n_{CH_4}=1mol\\ V_{CO_2}=1.24,79=24,79l\)