Nguyên tố nitrogen có hai đồng vị tự nhiên là \(\dfrac{14}{7}\)N và \(\dfrac{15}{7}\)N ,số loại phân tử N2 tồn tại bên trong khí quyển trái đất là? Giải thích?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Định hướng tư duy giải:
N2 công thức cấu tạo là: N≡N có công hóa trị là 3
N2 là đơn chất N có số oxi hóa là 0

Đáp án A
Định hướng tư duy giải:
N2 công thức cấu tạo là : N≡N
![]() có công hóa trị là 3
có công hóa trị là 3
N2 là đơn chất ![]() N có số oxi hóa là 0
N có số oxi hóa là 0

Phần trăm số nguyên tử AAg là 100% - 44% = 56%
Khối lượng nguyên tử trung bình: ¯¯¯¯A=x.A1+yA2100→107,88=44.109+56.A100→A=107

\(a,\overline{NTK}_B=\dfrac{10.18,89\%+11.81,11\%}{100\%}=10,8111\left(đ.v.C\right)\\ b,\overline{NTK}_{Ne}=\dfrac{20.91\%+22.\left(100\%-91\%\right)}{100\%}=20,18\left(đ.v.C\right)\\ c,\overline{NTK}_{Br}=\dfrac{79.54,5\%+81.\left(100\%-54,5\%\right)}{100\%}=79,91\left(đ.v.C\right)\\ d,\overline{NTK}_{Mg}=\dfrac{24.78,99\%+25.10\%+26.\left(100\%-78,89\%-10\%\right)}{100\%}\\ =24,3202\left(đ.v.C\right)\)
\(e,\overline{NTK}_{Ar}=\dfrac{36.0,34\%+38.0,06\%+40.\left(100\%-0,34\%+0,06\%\right)}{100\%}\\ =39,9852\left(đ.v.C\right)\\ f,\overline{NTK}_{Fe}=\dfrac{54.5,84\%+56.91,68\%+57.2,17\%+58.0,31\%}{100\%}\\ =55,9111\left(đ.v.C\right)\)

\(\overline{NTK}_N=\dfrac{99,63\%.14+0,37\%.15}{100\%}=14,0037\left(đ.v.C\right)\)

Gọi x,y lần lượt là phần trăm đồng vị của 12C và 13C
Ta có: \(\left\{{}\begin{matrix}x+y=100\\12.0,01x+13.0,01y=12,011\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=100-y\\0,12.\left(100-y\right)+0,13.y=12,011\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=98,9\%\\y=1,1\%\end{matrix}\right.\)
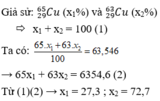
Số loại phân tử N2: 3
CTHH của các phân tử N2: \(^{14}_7N^{14}_7N\), \(^{15}_7N^{15}_7N\) và \(^{14}_7N^{15}_7N\)