X là hỗn hợp Al và Zn, Y là dung dịch HCL chưa rõ nồng độ.
- Thí nghiệm 1: Cho 21,65 gam X vào 2 lít Y được 10,08 lít H2 (đktc).
- Thí nghiệm 2: Cho 21,65gam X vào 3 lít Y được 12,32 lít H2 (đktc).
Tính nồng độ mol của dung dịch Y và khối lượng Al, Zn có trong hỗn hợp.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH:
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Thí nghiệm 1:
Ta có:
\(n_{H_2SO_4}=n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{0,4}{2}=0,2M\)
\(n_{Mg}+n_{Zn}=n_{H_2SO_4}=0,4\left(mol\right)\left(1\right)\)
Lại có: \(24n_{Mg}+65n_{Zn}=24,3\left(2\right)\)
Giải hệ hai phương trình (1) và (2) ta được:
\(\left\{{}\begin{matrix}n_{Mg}=0,04\left(mol\right)\\n_{Zn}=0,36\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,96\left(g\right)\\n_{Zn}=23,4\left(g\right)\end{matrix}\right.\)
Thí nghiệm 2:
Ta có:
\(n_{H_2SO_4}=n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(\Rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{0,5}{2}=0,25M\)
\(n_{Mg}+n_{Zn}=n_{H_2SO_4}=0,5\left(mol\right)\left(3\right)\)
Lại có: \(24n_{Mg}+65n_{Zn}=24,3\left(4\right)\)
Giải hệ hai phương trình (3) và (4) ta được:
\(\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Zn}=0,3\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Mg}=4,8\left(g\right)\\n_{Zn}=19,5\left(g\right)\end{matrix}\right.\)

Đáp án D
Nhận thấy ở hai thí nghiệm có lượng kim loại tham gia phản ứng như nhau, lượng HCl sử dụng lớn hơn lượng HCl sử dụng ở thí nghiệm 1 nhưng lượng H2 ở hai thí nghiệm thu được như nhau.
Do đó ở thí nghiệm 2 HCl phản ứng dư, thí nghiệm 1 có HCl phản ứng đủ hoặc dư.
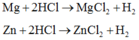
Có
![]()
Quan sát 4 đáp án nhận thấy chỉ có giá trị 0,3 là phù hợp.

* T N 1 : A l : a m o l N a : b m o l → H 2 O N a A l O 2 : b m o l H 2 A l B T e : n N a + 3 . n P b = b + 3 b = 2 . n H 2 = 0 , 48 → b = 0 , 12 * T N 2 : A l : 0 , 12 m o l N a : a m o l → H 2 O N a A l O 2 : 0 , 12 m o l N a O H : 0 , 03 m o l + . . . a = n N a = n N a O H + n N a A l O 2 = 0 , 15 → n A l ( T N 1 , T N 2 ) = 0 , 27 m o l → m A l = 7 , 29 g

Đáp án B
Thí nghiệm 1 cho m gam X vào H2O thu được V lít khí còn khí cho 2m gam vào NaOH thì thu được 3,5V lít tương đương khi cho m gam X vào NaOH thu được 1,75V lít.Do vậy trong X số mol Al nhiều hơn Na.
Gọi số mol của Na trong m gam X là x, suy ra khi cho m gam X vào H2O thì Al dư, nên Al phản ứng theo Na.
→ n H 2 = x + 3 x 2 = 2 x
Khi cho m gam X tác dụng với NaOH thu được 1,75V lít khí tức 3,5x mol khí. Lúc này cả Al và Na đều hết.
→ n A l = 3 , 5 x . 2 - x 3 = 2 x
Mặt khác cho 4m gam X vào HCl thu được 9V lít hay cho m gam X vào HCl thì thu được 2,25V lít hay 4,5x mol khí.
→ n M g = 4 , 5 x . 2 - x - 2 x . 3 2 = x
Vậy số mol Mg và Na bằng nhau

Đáp án B
Thí nghiệm 1 cho m gam X vào H2O thu được V lít khí còn khí cho 2m gam vào NaOH thì thu được 3,5V lít tương đương khi cho m gam X vào NaOH thu được 1,75V lít. Do vậy trong X số mol Al nhiều hơn Na.
Gọi số mol của Na trong m gam X là x, suy ra khi cho m gam X vào H2O thì Al dư, nên Al phản ứng theo Na.
→ n H 2 = x + 3 x 2 = 2 x
Khi cho m gam X tác dụng với NaOH thu được 1,75V lít khí tức 3,5x mol khí. Lúc này cả Al và Na đều hết.
→ n A l = 3 , 5 x . 2 - x 3 = 2 x
Mặt khác cho 4m gam X vào HCl thu được 9V lít hay cho m gam X vào HCl thì thu được 2,25V lít hay 4,5x mol khí
→ n M g = 4 , 5 x . 2 - x - 2 x . 3 2 = x
Vậy số mol Mg và Na bằng nhau.


Gọi nồng độ mol của dung dịch HCl là c (mol/lit) và khối lượng của hỗn hợp X là m (gam).
Theo phản ứng của Al và Zn với HCl, ta có phương trình phản ứng sau:
Al + HCl → AlCl3 + H2
Zn + 2HCl → ZnCl2 + H2
Tính nồng độ mol của dung dịch Y: Trong thí nghiệm 1, số mol H2 được sinh ra là 10,08 lít x 1 mol/lít = 10,08 mol. Trong thí nghiệm 2, số mol H2 được sinh ra là 12,32 lít x 1 mol/lít = 12,32 mol.
Ta thấy tỷ lệ số mol H2 và thể tích dung dịch HCl là như nhau trong cả hai thí nghiệm, do đó ta có phương trình:
10,08 mol H2 / 2 lít HCl = 12,32 mol H2 / 3 lít HCl
Từ đó, ta tính được nồng độ mol của dung dịch HCl (c):
10,08 mol H2 / 2 lít HCl = c mol/lít
c = 5,04 mol/lít
Tính khối lượng của Al và Zn trong hỗn hợp X: Trong phản ứng, mỗi mol Al tạo ra 3 mol H2 và mỗi mol Zn tạo ra 1 mol H2.
Với số mol H2 đã tính được từ thí nghiệm 1 (10,08 mol) và thí nghiệm 2 (12,32 mol), ta có:
10,08 mol H2 / 3 = mAl / 26,98 g/mol
mAl = 10,08 mol H2 / 3 x 26,98 g/mol
mAl = 89,79 g
12,32 mol H2 / 1 = mZn / 65,38 g/mol
mZn = 12,32 mol H2 x 65,38 g/mol
mZn = 806,90 g
Vậy, nồng độ mol của dung dịch Y là 5,04 mol/lít và khối lượng Al và Zn trong hỗn hợp X lần lượt là 89,79 g và 806,90 g.