20,8 gam hỗn hợp Fe, Cu phản ứng vừa đủ với oxygen tạo thành 28g hỗn hợp oxit. tính thể tích oxi phản ứng(đkc) và % khối lượng mỗi kim loại trong hỗn hợp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) nCl2=7,28/22,4=0,325(mol)
=> mCl2=0,325.71=23,075(mol)
=> m(muối)= m(hh)+ mCl2= 10,45+23,075=33,525(g)
b) PTHH: 2 Al + 3 Cl2 -to-> 2 AlCl3
a__________1,5a(mol)
Cu + Cl2 -to-> CuCl2
b___b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}27a+64b=10,45\\1,5a+b=0,325\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,15\\b=0,1\end{matrix}\right.\)
=> mCu=0,1.64=6,4(g)
=>%mCu= (6,4/10,45).100=61,244%
=>%mAl=38,756%

\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ \Rightarrow n_{Zn}=n_{H_2}=\dfrac{3,7185}{24,79}=0.,15(mol)\\ \Rightarrow m_{Zn}=0,15.65=9,75(g)\\ \Rightarrow \%_{Zn}=\dfrac{9,75}{10}.100\%=97,5\%\\ \Rightarrow \%_{Cu}=100\%-97,5\%=2,5\%\\ b,n_{HCl}=2n_{H_2}=0,3(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{0,3.36,5}{14\%}=78,21(g)\)

a) \(m_X=0,1\cdot64+0,2\cdot27+0,3\cdot24=19\left(g\right)\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,1\cdot64\cdot100}{19}=34\%\)
\(\Rightarrow\%m_{Al}=\dfrac{0,2\cdot27\cdot100}{19}=28\%\)
\(\Rightarrow\%m_{Mg}=100\%-34\%-28\%=38\%\)
b) \(Cu+2HCl\rightarrow CuCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
\(Mg+2HCl\rightarrow MgCl_2+H_2\) (3)
\(n_{HCl\left(1\right)}=2n_{Cu}=2\cdot0,1=0,2\left(mol\right)\)
\(n_{HCl\left(2\right)}=\dfrac{6\cdot n_{Al}}{2}=3\cdot0,2=0,6\left(mol\right)\)
\(n_{HCl\left(3\right)}=2n_{Mg}=2\cdot0,3=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=\left(0,2+0,6+0,6\right)\cdot36,5=51,1\left(g\right)\)
\(n_{H_2\left(1\right)}=n_{Cu}=0,1\left(mol\right);n_{H_2\left(2\right)}=\dfrac{3\cdot0,2}{2}=0,3\left(mol\right);n_{H_2\left(3\right)}=n_{Mg}=0,3\left(mol\right)\)
\(V_{H_2\left(dkc\right)}=\left(0,1+0,3+0,3\right)\cdot24,79=17,353\left(l\right)\)

Chọn đáp án C
n H C l = 2 n O o x i t = 2 3 , 33 - 2 , 13 16 = 0,15 (mol)
→ V d d H C l = 0 , 15 0 , 2 = 0,075 (lít)
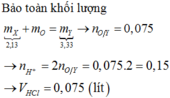
\(BTKL:m_{O_2}=28-20,8=7,2g\\V_{O_2}=\dfrac{7,2:32}{22,4}=\dfrac{9}{896}l\\ 3Fe+2O_2\xrightarrow[]{t^0}Fe_3O_4\\ 2Cu+O_2\xrightarrow[]{t^0}2CuO\\ n_{Fe}=a;n_{Cu}=b\\ \Rightarrow\left\{{}\begin{matrix}56a+64b=20,8\\\dfrac{1}{3}a232+80b=28\end{matrix}\right.\\ \Rightarrow a=\dfrac{3}{11};b=\dfrac{19}{220}\\ \%m_{Fe}=\dfrac{\left(3:11\right)56}{20,8}\cdot100=73,43\%\\ \%m_{Cu}=100-73,43=26,57\%\)