Nếu không dùng cân, làm thế nào có thể biết được 24,79 lít khí N2 nặng hơn 24,79 lít khí H2 bao nhiêu lần (ở cùng điều kiện nhiệt độ, áp suất)?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn D
Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng là tỉ lệ về số mol.
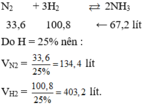

Giả sử hỗn hợp có x mol O2 và y mol N2
Ta có: \(\overline{M}=\dfrac{32x+28y}{x+y}>29\)
=> 32x + 28y > 29x + 29y
=> 3x > y
=> \(\dfrac{x}{y}>\dfrac{1}{3}\)
Vậy cần trộn O2 và N2 sao cho tỉ lệ \(\dfrac{V_{O_2}}{V_{N_2}}>\dfrac{1}{3}\) để thu được hỗn hợp Y nặng hơn không khí

H=50%H=50%
Giải thích các bước giải:
3N2+H2t∘,p,xt−−−→2NH33N2+H2→t∘,p,xt2NH3
Xét: 17,53>5⇒17,53>5⇒ Hiệu suất tính theo N2N2
Vì các thể tích khí đo trong cùng điều kiện nhiệt độ và áp suất nên tỉ lệ thể tích cũng là tỷ lệ số mol
dA/H2 =5 —> MA = 10
BTKL —> mA = 175
—> nA = 17,5
Gọi nN2 phản ứng là a
—> nH2 phản ứng = 3a; nNH3 = 2a mol
—> nN2 dư = 5 - a; nH2 dư = 17,5 - 3a mol
—> 5 - a + 17,5 - 3a + 2a = 17,5
—> a = 2,5
—> H = 2,5/5 . 100% = 50%

\(M_A=5.2=10\left(g/mol\right)\)
Do các khí đo ở cùng điều kiện nhiệt độ và áp suất nên tỉ lệ thể tích cũng là tỉ lệ mol
Chọn \(\left\{{}\begin{matrix}n_{H_2}=17,5\left(mol\right)\\n_{N_2}=5\left(mol\right)\end{matrix}\right.\)
Gọi \(n_{N_2\left(p\text{ư}\right)}=a\left(mol\right)\left(0< a< 5\right)\)
PTHH: \(N_2+3H_2\xrightarrow[]{t^o,p,xt}2NH_3\)
a---->3a---------->2a
Xét tỉ lệ: \(5< \dfrac{17,5}{3}\Rightarrow\) Hiệu suất phản ứng tính theo N2
Ta có: \(n_A=5+17,5+2a-a-3a=22,5-2a\left(mol\right)\)
Theo ĐLBTKL: \(m_A=5.28+17,5.2=175\left(g\right)\)
\(\Rightarrow M_A=\dfrac{175}{22,5-2a}=10\Leftrightarrow a=2,5\left(TM\right)\)
\(\Rightarrow H=\dfrac{2,5}{5}.100\%=50\%\)

Ta thấy tỉ lệ về thể tích cùng là tỉ lệ về số mol:
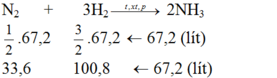
Tỉ lệ số mol cũng chính là tỉ lệ thể tích
Theo pt:
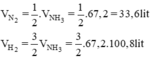
Do hiệu suất của phản ứng là 25% nên thể tích của nitơ và hiđro cần lấy là:
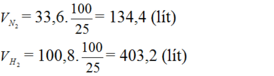

a) Giả sử các khí đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
Gọi số mol N2, H2 ban đầu là a, b (mol)
=> a + b = 50 (1)
Gọi số mol N2 pư là x (mol)
PTHH: N2 + 3H2 --to,xt--> 2NH3
Trc pư: a b 0
Pư: x---->3x----------->2x
Sau pư (a-x) (b-3x) 2x
=> a + b - 2x = 44
=> x = 3 (mol)
Có \(n_{N_2\left(sau.pư\right)}=a-x=44.25\%=11\left(mol\right)\)
=> a = 14 (mol)
=> b = 36 (mol)
\(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{14}{50}.100\%=28\%\\\%V_{H_2}=\dfrac{36}{50}.100\%=72\%\end{matrix}\right.\)
Y chứa \(\left\{{}\begin{matrix}N_2:11\left(mol\right)\\H_2:27\left(mol\right)\\NH_3:6\left(mol\right)\end{matrix}\right.\)
Z chứa \(\left\{{}\begin{matrix}N_2:11\left(mol\right)\\H_2:27\left(mol\right)\\NH_3:6\left(mol\right)\\N_2O:6\left(mol\right)\end{matrix}\right.\)
\(Z\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{11}{11+27+6+6}.100\%=22\%\\\%V_{H_2}=\dfrac{27}{11+27+6+6}.100\%=54\%\\\%V_{NH_3}=\dfrac{6}{11+27+6+6}.100\%=12\%\\\%V_{N_2O}=\dfrac{6}{11+27+6+6}.100\%=12\%\end{matrix}\right.\)
b)
11,2 lít hh Z ở đktc chứa \(\left\{{}\begin{matrix}n_{N_2}=\dfrac{11,2.22\%}{22,4}=0,11\left(mol\right)\\n_{H_2}=\dfrac{11,2.54\%}{22,4}=0,27\left(mol\right)\\n_{NH_3}=\dfrac{11,2.12\%}{22,4}=0,06\left(mol\right)\\n_{N_2O}=\dfrac{11,2.12\%}{22,4}=0,06\left(mol\right)\end{matrix}\right.\)
=> mZ = 0,11.28 + 0,27.2 + 0,06.17 + 0,06.44 = 7,28 (g)
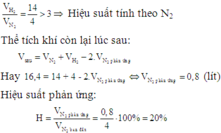
\(V_{N_2}=V_{H_2}\\ \Rightarrow n_{N_2}=n_{H_2}=a\left(mol\right)\left(a>0\right)\\ m_{N_2}=28a\left(g\right);m_{H_2}=2a\left(g\right)\\ Ta.có:\dfrac{m_{N_2}}{m_{H_2}}=\dfrac{28a}{2a}=14\)
Vậy không dùng cân, bằng các CT tính toán ta thấy được 24,79 lít khí N2 sẽ nặng gấp 14 lần 24,79 lít khí H2 ở cùng đk nhiệt độ, áp suất