Hòa tan m gam Fe3O4 cần dùng 400 mL dung dịch H2SO4 loãng 0,025M. Viết PTPU và tính V?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\\ PTHH:Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ n_{H_2SO_4}=3.0,05=0,15\left(mol\right)\\ m=m_{ddH_2SO_4}=\dfrac{0,15.98.100}{4,9}=300\left(g\right)\)

\(Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{Mg}=n_{H_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right);n_{HCl}=2.0,1=0,2\left(mol\right)\\ m=m_{Mg}=0,1.24=2,4\left(g\right);V=V_{ddHCl}=\dfrac{0,2}{0,4}=0,5\left(l\right)\)

nAl = 5.4/27 = 0.2 (mol)
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
0.2____0.3_________________0.3
VH2 = 0.3*22.4 = 6.72(l)
CM H2SO4 = 0.3/0.1 = 3 M
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(\Rightarrow n_{H_2}=0,3mol=n_{H_2SO_4}\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,3\cdot22,4=6,72\left(l\right)\\C_{M_{H_2SO_4}}=\dfrac{0,3}{0,1}=3\left(M\right)\end{matrix}\right.\)

Đáp án C
Vì số mol của FeO bằng số mol của Fe2O3 nên ta coi hỗn hợp là Fe3O4
Ta có:
Fe3O4 +4H2SO4 → FeSO4 +Fe2(SO4)3 +4H2O
0,02 0,02
Trong 100 ml X sẽ có 0,01 mol FeSO4 nên:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
→ nKMnO4 = 0,02 mol → VKMnO4 = 0,02/0,1 = 0,2 l

a, gọi a= nFe
b= nFeO
=> 56a + 72b= 12,8 (1)
Fe +H2SO4 -> FeSO4 +H2
a b b a
FeO +H2SO4 -> FeSO4 +H2O
b b b
a=nH2 = 2,24/22,4= 0,1 mol
từ (1) => b= 0,1
mFe= 56.0,1=5,6(g)
m FeO = 72.0,1= 7,2(g)
b, nH2SO4 (bđ) = 0,25 mol
nH2SO4 pứ = a+b =0,2 mol
=> nH2SO4 dư = 0,25-0,2=0,05 mol
2NaOH +H2SO4 -> Na2SO4 +2H2O
0,1 0,05
V(NaOH)= 0,1/ 1= 0,1 lit =100ml
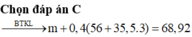


\(n_{H_2SO_4}=0,4.0,025=0,01\left(mol\right)\)
PT: \(Fe_3O_4+4H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+FeSO_4+4H_2O\)
Theo PT: \(n_{Fe_3O_4}=\dfrac{1}{4}n_{H_2SO_4}=0,0025\left(mol\right)\Rightarrow m_{Fe_3O_4}=0,0025.232=0,58\left(g\right)\)