(1 điểm). Cho 9,2 gam hỗn hợp gồm Zn và Al phản ứng hoàn toàn với lượng dư dung dịch H2SO4 đặc, nóng thu được 5,6 lít khí SO2 (ở đktc, là sản phẩmkhử duy nhất). Khối lượng Al có trong hỗn hợp ban đầu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A
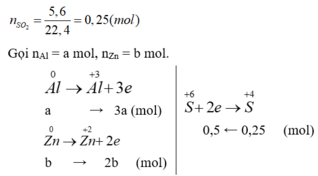
Ta có: m h h = 9 , 2 g → 27a + 65b = 9,2 (*)
Bảo toàn số mol electron có: 3a + 2b = 0,5 (**)
Giải (*), (**): a = b = 0,1 mol.
m A l = 0 , 1 . 27 = 2 , 7 g a m

Đáp án A.
Gọi nAl = a mol, nZn = b mol.

Ta có: 27a + 65b = 9,2 (*)
3a + 2b = 0,5 (**)
Giải (*), (**): a = b = 0,1 mol.
mAl = 0,1.27 = 2,7 gam

Đáp án A.
Gọi nAl = a mol, nZn = b mol.

Ta có: 27a + 65b = 9,2 (*)
3a + 2b = 0,5 (**)
Giải (*), (**): a = b = 0,1 mol.
m muối = mKl + M gốc axit. ne/2
= 3,92 + 96. 0,25 = 33,2 g

Đáp án C
Phản ứng hoàn toàn thu được
sản phẩm + KOH ⇒ H2 ⇒ Al dư.
Ta có phản ứng:
8Al + 3Fe3O4 ![]() 4Al2O3 + 9Fe.
4Al2O3 + 9Fe.
Với nAl dư = 2nH2÷3 = 0,02 mol.
Xem hỗn hợp X gồm: nAl = 0,02
nAl2O3 = a || nFe = b ta có:
PT bảo toàn e với SO2:
3nAl + 3nFe = 2nSO2
Û nFe = b = 0,0225
⇒ nAl2O3 = 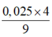 = 0,01.
= 0,01.
Bảo toàn khối lượng
mHỗn hợp ban đầu = mAl + mAl2O3 + mFe
= 2,82 gam.
Bảo toàn nguyên tố Al
⇒ ∑nAl ban đầu = 0,02 + 0,01×2 = 0,04 mol.
⇒ %mAl = 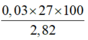
= 38,298%


Số mol S O 2 = 1,5x + 0,03 = 0,06375→ x = 0,0225 mol
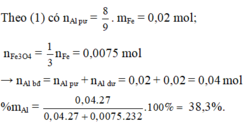
⇒ Chọn C.

Đáp án C
8 Al + 3 Fe 3 O 4 → t o 4 Al 2 O 3 + 9 Fe
Vì phản ứng xảy ra hoàn toàn và hòa tan A vào dung dịch NaOH thu được khí nên A gồm Fe, A12O3 và Al dư.


Đáp án : A
nH2 = 0,25 mol; nSO2 = 0,3 mol
2H+ + 2e → H2 S+6 + 2e → S+4
0,5 <-- 0,25 0,6 <-- 0,3
nFe = 0,6 – 0,5 = 0,1 mol
=> mFe = 5,6g

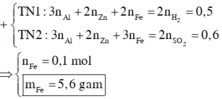

Gọi x,y lần lượt là số mol của Zn và Al
Theo đề ta có mHỗnhợp=65x+27y=9,2(1)
nSO2=5,6:22,4=0,25mol
BTE:2x+3y=2.0,25=0,5(2)
Từ (1) và (2) => x=0,1;y=0,1
mAl=0,1.27=2,7g
Gọi x,y lần lượt là số mol của Zn và Al
Theo đề ta có mHỗnhợp=65x+27y=9,2(1)
nSO2=5,6:22,4=0,25mol
BTE:2x+3y=2.0,25=0,5(2)
Từ (1) và (2) => x=0,1;y=0,1
mAl=0,1.27=2,7g
Chúc bạn học tốt!!!