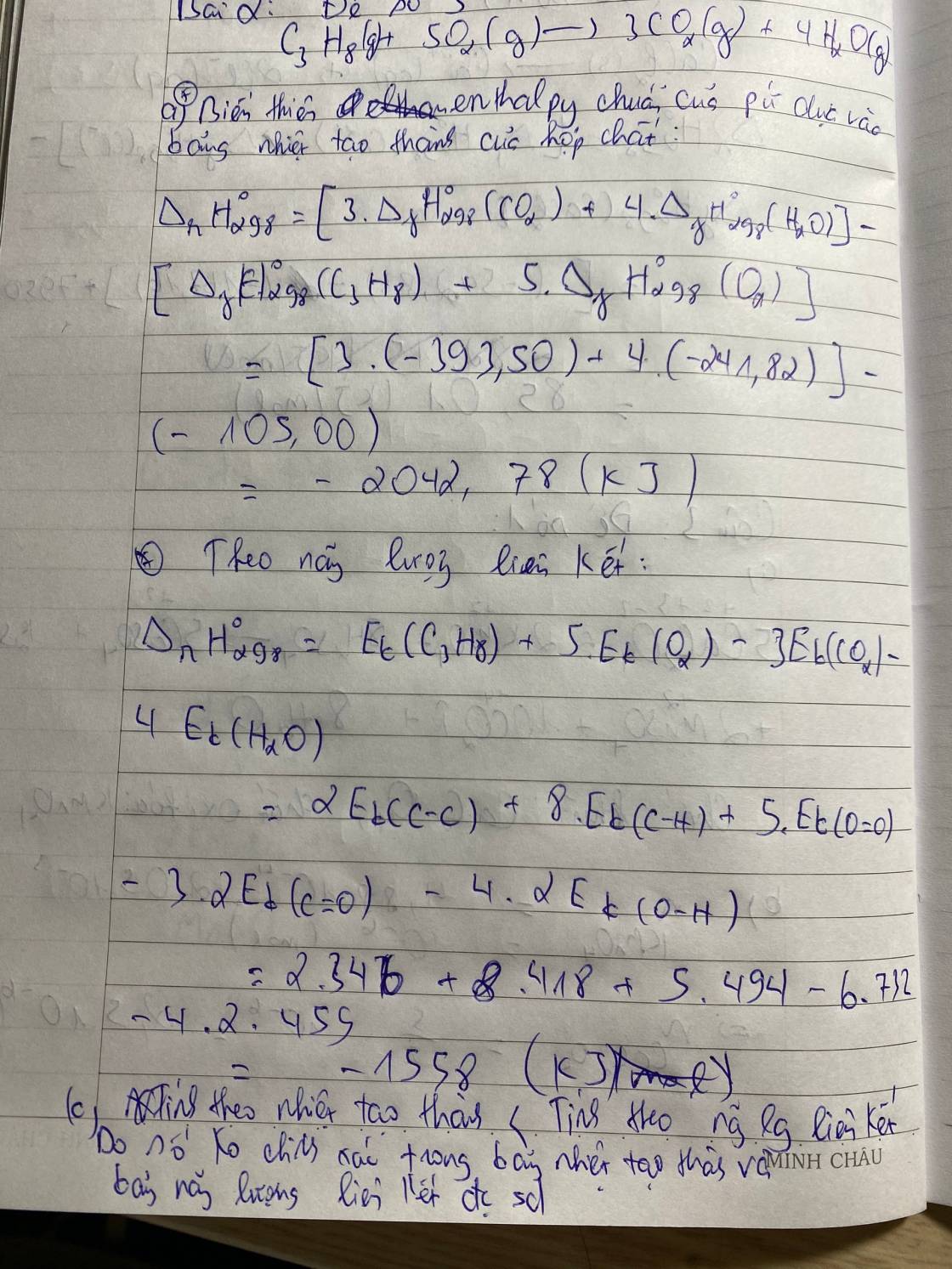(2 điểm). Xét quá trình đốt cháy khí propane C3H8(g):
C3H8(g) + 5O2(g) \(\rightarrow\) 3CO2(g) + 4H2O(g)
a) Tính biến thiên enthalpy chuẩn của phản ứng dựa vào bảng nhiệt tạo thành của hợp chất và dựa vào dựa vào bảng năng lượng liên kết.
Biết nhiệt tạo thành của C3H8(g); CO2(g) và H2O(g) lần lượt là : –105,00; –393,50 và –241,82 kJ/mol.
Biết EC-H = 418 kJ/mol; EC-C = 346 kJ/mol; EO=O = 494 kJ/mol; EC=O = 732 kJ/mol và EO-H = 459 kJ/mol.
b) So sánh hai giá trị đó và nếu có sự khác biệt, hãy giải thích tại sao lại có sự khác biệt đó ?