Xét phản ứng H2 + Cl2 → 2HCl
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị sau:
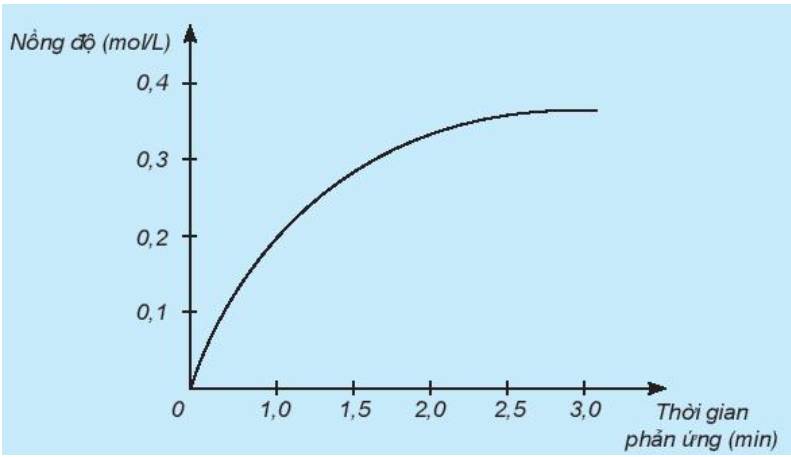 a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
b) Nêu đơn vị của tốc độ phản ứng trong trường hợp này.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

b) Từ đồ thị ta thấy: Lúc đầu số mol sản phẩm bằng 0, theo thời gian, số mol chất tham gia (hydrogen, iodine) giảm dần, số mol chất sản phẩm (hydrogen iodide) tăng dần, đến khi số mol của các chất hydrogen, iodine, hydrogen iodide không thay đổi nữa.
c) Biểu thức định luật tác dụng khối lượng:
- Đối với phản ứng thuận:
vthuận = \({\rm{k}}{\rm{.}}{{\rm{C}}_{{{\rm{H}}_{\rm{2}}}}}{\rm{.}}{{\rm{C}}_{{{\rm{I}}_{\rm{2}}}}}\)
- Đối với phản ứng nghịch:
vnghịch = \({\rm{k'}}{\rm{.C}}_{{\rm{HI}}}^2\)
Dự đoán:
- Ban đầu tốc độ phản ứng thuận giảm dần, sau một thời gian tốc độ phản ứng thuận không thay đổi theo thời gian.
- Ban đầu tốc độ phản ứng nghịch tăng dần, sau một thời gian tốc độ phản ứng nghịch không thay đổi theo thời gian.
d) Tại thời điểm phản ứng thuận nghịch đạt tới trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch thì số mol các chất trong hệ phản ứng không thay đổi nữa.

Đồ thị a biểu diễn sự biến đổi tốc độ phản ứng thuận theo thời gian.
Đồ thị b biểu diễn sự biến đổi tốc độ phản ứng nghịch theo thời gian.
Đồ thị c biểu diễn trạng thái cân bằng hoá học.

tham khảo
Đồ thị là đồ thị hàm sin. Vật bắt đầu chuyển động tại vị trí có li độ lớn nhất, sau đó li độ giảm dần đến 0 rồi đến li độ nhỏ nhất. Li độ từ giá trị nhỏ nhất lại tăng dần đến 0 rồi đến giá trị lớn nhất. Sau đó, quá trình lặp lại, li độ từ giá trị lớn nhất giảm dần, … Sự thay đổi diễn ra tuần hoàn, theo chu kì.

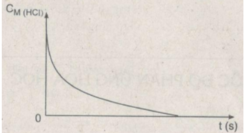
Dạng đồ thị biểu diễn sự phụ thuộc của nồng độ axit HCL theo thời gian

Sau một khoảng thời gian, màu tím của hỗn hợp khí không thay đổi, chứng tỏ nồng độ I2 không thay đổi. Nghĩa là sau một thời gian, lượng I2 sinh ra từ phản ứng nghịch và lượng I2 mất đi từ phản ứng thuận bằng nhau. Hay tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. Do đó đồ thị (a) thể hiện đúng Ví dụ 2.
Đường màu xanh biểu diễn tốc độ phản ứng nghịch. Ban đầu phản ứng, chưa sinh ra HI nên tốc độ phản ứng nghịch bằng 0. Sau một thời gian, lượng HI sinh ra càng nhiều, tốc độ phản ứng nghịch tăng. Sau đó, lượng HI sinh ra từ phản ứng thuận bằng lượng HI mất đi từ phản ứng nghịch, tức tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch nên đường đồ thị màu xanh trùng với đường đồ thị màu đỏ.

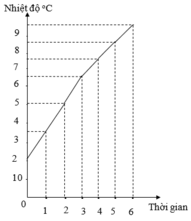
a) Khi đun, nhiệt độ của nước tăng lên.
b) - Biểu diễn đúng các điểm;
- Vẽ đúng đồ thị.
a) Theo thời gian, nồng độ có xu hướng tăng dần
=> Đồ thị mô tả sự thay đổi nồng độ theo thời gian của sản phẩm HCl
b) Đơn vị của tốc độ phản ứng trong trường hợp này là phút (min).