cho 30g hh gồm Fe và Ag hoà tan hoàn vào dung dịch có 300ml CuCl2,2M tính khối lượng của mỗi kim loại trong hh Giúp tôi với xin cảm ơn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi nFe=a(mol);nM=b(mol)⇒56a+Mb=9,6(1)
Fe+2HCl→FeCl2+H2
M+2HCl→MCl2+H2
nH2=a+b=0,2⇒a=0,2−b
Ta có :
56a+Mb=9,656a+Mb=9,6
⇔56(0,2−b)+Mb=9,6
⇔Mb−56b=−1,6
⇔b(56−M)=1,6
⇔b=1,656−M
Mà 0<b<0,20<b<0,2
Suy ra : 0<1,656−M<0,20<1,656−M<0,2
⇔M<48(1)
M+2HCl→MCl2+H2
nM=nH2<5,622,4=0,25
⇒MM>4,60,25=18,4
+) Nếu M=24(Mg)
Ta có :
56a+24b=9,656a+24b=9,6
a+b=0,2a+b=0,2
Suy ra a = 0,15 ; b = 0,05
mFe=0,15.56=8,4(gam)
mMg=0,05.24=1,2(gam)
+) Nếu M=40(Ca)
56a+40b=9,656a+40b=9,6
a+b=0,2
Suy ra a = b = 0,1
mCa=0,1.40=4(gam)
mFe=0,1.56=5,6(gam)

\(Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\\ a,\%m_{Fe}=\dfrac{0,02.56}{4,36}.100\approx25,688\%\\ \Rightarrow\%m_{Ag}\approx74,312\%\\ b,Ta.thấy:2,18=\dfrac{1}{2}.4,36\\ \Rightarrow m_{hh\left(câuB\right)}=\dfrac{1}{2}.m_{hh\left(câuA\right)}\\ n_{Fe}=\dfrac{0,02}{2}=0,01\left(mol\right)\\ n_{Ag}=\dfrac{2,18-0,01.56}{108}=0,015\left(mol\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ 2Ag+Cl_2\rightarrow\left(t^o\right)2AgCl\\ n_{Cl_2}=\dfrac{3}{2}.n_{Fe}+\dfrac{1}{2}.n_{Ag}=\dfrac{3}{2}.0,01+\dfrac{1}{2}.0,015=0,0225\left(mol\right)\\ \Rightarrow V_{Cl_2\left(đktc\right)}=0,0225.22,4=0,504\left(l\right)\)

Gọi số mol Cu, Fe là a, b (mol)
=> 64a + 56b = 17,6 (1)
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
b-------------------------------->1,5b
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
a--------------------------->a
=> a + 1,5b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,2 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,1.64}{17,6}.100\%=36,36\%\\\%m_{Fe}=\dfrac{0,2.56}{17,6}.100\%=63,64\%\end{matrix}\right.\)

Giả sử hh hết
MgO + 2HCl \(\rightarrow\) MgCl2 + H2O (1)
0,1 \(\rightarrow\) 0,2 (mol)
Fe2O3 + 6HCl \(\rightarrow\) 2FeCl3 + 3H2O (2)
0,1 \(\rightarrow\) 0,6 (mol)
nHCl pư = 0,8 > 0,4 (mol)
=> Giả sử sai
=|>HCl hết
Gọi số mol MgO , Fe2O3 pư lần lượt là x , y
Theo pt (1),(2) nHCl = 2x + 6y = 0,4 (mol) (l)
Tỉ lệ số mol của MgO : Fe2O3 ban đầu là tỉ lệ MgO : Fe2O3 pư
=> \(\frac{x}{y}\) = \(\frac{0,1}{0,1}\) = 1 (ll)
Giải hệ pt (l) ,(ll)=> x=y=0,05
=|> Mmuối = 0,05 . 95 + 0,05 . 2 . 162,5 = 21 (g)

a, \(m_{hh}=m_{Al}+m_{Fe}=27n_{Al}+56n_{Fe}=11,1\left(I\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PTHH : \(\dfrac{3}{2}n_{Al}+n_{Fe}=n_{H2}=0,3\left(II\right)\)
- Giair 1 và 2 => \(\left\{{}\begin{matrix}n_{Al}=0,1\\n_{Fe}=0,15\end{matrix}\right.\) mol
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=2,7g\left(24,32\%\right)\\m_{Fe}=8,4g\left(75,68\%\right)\end{matrix}\right.\)
b, - Theo PTHH : \(n_{H2SO4du}=n_{H2SO4}-n_{H2SO4pu}=0,325mol\)
\(\Rightarrow m_{H2SO4du}=31,85g\)
Ta có ; \(m_{dd}=m_{ddH2SO4}+m_{hh}-m_{H2}=255,5g\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{H2SO4}=\dfrac{m}{mdd}.100\%=12,46\%\\C\%_{Al2\left(SO4\right)3}=\dfrac{m}{mdd}.100\%=6,7\%\\C\%_{FeSO4}=\dfrac{m}{mdd}.100\%=8,9\%\end{matrix}\right.\)
Vậy ...
2Al+3H2SO4→Al2(SO4)3+3H2
Fe+H2SO4→FeSO4+H2
a,nH2=\(\dfrac{6,72}{22,4}\)=0,3(mol)
Gọi số mol của Al là x, số mol của Fe là y
Ta có :
27x+56y=11,1 (1)
1,5a+b=0,3 (2)
Từ (1),(2) ⇒x=0,1 ; y=0,15
%mAl=\(\dfrac{0,1.27}{11,1}.100\)=24,32%
%mFe=100%−24,32%=75,68%
b,nH2SO4=\(\dfrac{245.25\%}{98}\)=0,625(mol)
⇒nH2SO4.trong.Y=0,625−0,3=0,325(mol)
mdd(spu)=11,1+245−0,3.2=255,5(g)
nAl2(SO4)3=0,05(mol)
nFeSO4=0,15(mol)
⇒C%H2SO4=12,47%
C%Al2(SO4)3=6,2%
C%FeSO4=8,92%
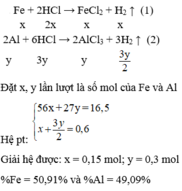
Em xem lại đề nha