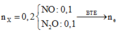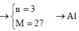Bài 5: Xác định tên kim loại a) Khi cho 19,2g kim loại M hoá trị 2 vào dd HNO3 thì thu được 4.48 lít khí NO(đktc) b) Cho 4,05g kim loại M hoá trị 3 vào dd HNO3 đặc nóng thì thu được 10,8 lít khí NO2(đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1. Gọi KL cần tìm là A.
PT: \(A+H_2SO_4\rightarrow ASO_4+H_2\)
Ta có: \(n_A=\dfrac{32,5}{M_A}\left(mol\right)\)
\(n_{ASO_4}=\dfrac{80,5}{M_A+96}\left(mol\right)\)
Theo PT: \(n_A=n_{ASO_4}\Rightarrow\dfrac{32,5}{M_A}=\dfrac{80,5}{M_A+96}\Rightarrow M_A=65\left(g/mol\right)\)
→ A là Zn.
2. Gọi KL cần tìm là A
Ta có: \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(2A+O_2\underrightarrow{t^o}2AO\)
Theo PT: \(n_A=2n_{O_2}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{19,2}{0,3}=64\left(g/mol\right)\)
→ A là đồng.

1)
Zn + 2HCl --> ZnCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
Zn + 4HNO3 --> Zn(NO3)2 + 2NO2 + 2H2O
2)
TN2:
\(n_{NO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Zn + 4HNO3 --> Zn(NO3)2 + 2NO2 + 2H2O
_____0,05<--------------------------0,1
=> nZn = 0,05 (mol)
TN1:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
____0,05--------------------->0,05
2Al + 6HCl --> 2AlCl3 + 3H2
0,1<-----------------------0,15
=> m = 0,05.65 + 0,1.27 = 5,95(g)

\(\text{Ta có }n_M=\dfrac{10,8}{M_M}\left(mol\right);n_{N_2O}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:8M+30HNO_3\rightarrow8M\left(NO_3\right)_3+3N_2O+15H_2O\\ \Rightarrow n_M=\dfrac{8}{3}n_{N_2O}=0,4\left(mol\right)\\ \Rightarrow\dfrac{10,8}{M_M}=0,4\\ \Rightarrow M_M=27\)
Vậy M là nhôm (Al)

\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(2A+2nH_2O\rightarrow2A\left(OH\right)_n+nH_2\)
\(\dfrac{0.1}{n}........................0.05\)
\(M_A=\dfrac{3.9}{\dfrac{0.1}{n}}=39n\)
Với : \(n=1\rightarrow A=39\)
\(A:K\)
\(m_{KOH}=0.1\cdot56=5.6\left(g\right)\)
\(m_{ddX}=3.9+46.2-0.05\cdot2=50\left(g\right)\)
\(C\%_{KOH}=\dfrac{5.6}{50}\cdot100\%=11.2\%\)
\(b.\)
\(K_2O+H_2O\rightarrow2KOH\)
\(0.1....................0.2\)
\(m_{KOH}=0.2\cdot56=11.2\left(g\right)\)
\(m_{dd_X}=\dfrac{11.2}{28\%\%}=40\left(g\right)\)

Sửa đề : khí NO
\(n_{NO}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\text{Bảo toàn e : }\)
\(n_M=\dfrac{3n_{NO}}{n}=\dfrac{0.6}{n}\left(mol\right)\)
\(M_M=\dfrac{19.2}{\dfrac{0.6}{n}}=32n\left(\dfrac{g}{mol}\right)\)
\(BL:n=2\Rightarrow M=64\)
\(Mlà:Cu\)
Ta có: nNO2=\(\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
PTHH: \(3M+4HNO_3->3M\left(NO_3\right)_n+nNO+2H_2O\)
Dựa vào pthh tính đưuọc nM=\(\dfrac{0.6}{n}\)
Ta có: \(M_M=\dfrac{19.2}{\dfrac{0.6}{n}}=32n\)
Vì M là kim loại nên n có thể = 1,2,3
Tìm n=2 là hợp lý nhất=> n=2 thì M=64. Vậy M là Cu

a)
M + 2HCl → MCl2 + H2
nH2 = \(\dfrac{3,584}{22,4}=\)0,16 mol => nM = 0,16 mol
<=> MM = \(\dfrac{3,84}{0,16}\)= 24 (g/mol) => M là magie (Mg).
b) 8Mg + 20HNO3 → 8Mg(NO3) + 2NO + N2 + 10H2O
Từ tỉ lệ phương trình , gọi số mol N2 là x => nNO = 2x mol
=> V(NO + N2) =3x.22,4 =1,344
<=> x =0,02
=> VN2 = 0,02.22,4 =0,448 lít , VNO= 0,04.22,4 = 0,896 lít

a, PTHH:
\(A+2HCl\rightarrow ACl_2+H_2\left(1\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(2\right)\)
\(AlCl_3+4NaOH\rightarrow NaAlO_2+3NaCl+2H_2O\)
b, Ta có \(n_{AlCl_3}=n_{NaAlO_2}=\dfrac{2,7}{82}=0,03\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=n_{AlCl_3}=0,03\left(mol\right)\\n_{H_2\left(2\right)}=\dfrac{3}{2}n_{AlCl_3}=0,045\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=27.0,03=0,81\left(g\right)\\n_A=n_{H_2\left(1\right)}=\dfrac{1,68}{22,4}-n_{H_2\left(2\right)}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_A=2,49-0,81=1,68\left(g\right)\\n_A=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow M_A=\dfrac{1,68}{0,03}=56\left(g/mol\right)\Rightarrow A\) là \(Fe\)
c, \(m_{\text{muối}}=m_{FeCl_2}+m_{AlCl_3}\)
\(=127.n_{Fe}+133,5.n_{Al}\)
\(=127.0,03+133,5.0,03=7,815\left(g\right)\)

Đáp án D
Bảo toàn e : 2nM = nNO2 => nM = 0,0875 mol
=> Mkimloại = 64g => Kim loại cần tìm là Cu