pha 100ml dung dịch H2SO4 20% từ H2SO4 98%(giúp mình với mai mình phải thực hành bài này rui)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Cách tiến hành khi pha loãng
Khi pha loãng lấy 717,6 ml H2O vào ống đong hình trụ có thể tích khoảng 2 lít. Sau đó cho từ từ 100ml H2SO4 98% vào lượng nước trên, đổ axit chảy theo một đũa thủy tinh, sau khi đổ vài giọt nên dùng đũa thủy tinh khuấy nhẹ đều. Không được đổ nước vào axit 98%, axit sẽ bắn vào da, mắt..và gây bỏng rất nặng

Thể tích nước cần dùng để pha loãng.
Khối lượng của 100ml dung dịch axit 98%
100ml × 1,84 g/ml = 184g
Khối lượng H2SO4 nguyên chất trong 100ml dung dịch trên: 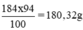
Khối lượng dung dịch axit 20% có chứa 180,32g H2SO4 nguyên chất: 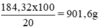
Khối lượng nước cần bổ sung vào 100ml dung dịch H2SO4 98% để có được dung dịch 20%: 901,6g – 184g = 717,6g
Vì D của nước là 1 g/ml nên thể tích nước cần bổ sung là 717,6 ml.

\(n_{HCl}=0,1.0,1=0,01\left(mol\right);n_{HCl}=0,3.0,04=0,012\left(mol\right)\)
Dung dịch gồm H+ và Cl-
\(n_{H^+}=0,01+0,012=0,022\left(mol\right)\)
=> \(\left[H^+\right]=\dfrac{0,022}{0,4}=0,055M\)
\(n_{Cl^-}=0,01+0,012=0,022\left(mol\right)\)
=>\(\left[Cl^-\right]=\dfrac{0,022}{0,4}=0,055M\)
Trộn 100ml dung dịch HNO3 0.1M với 400ml dung dịch H2SO4 0.03M
\(n_{HNO_3}=0,1.0,1=0,01\left(mol\right);n_{H_2SO_4}=0,04.0,3=0,012\left(mol\right)\)
Dung dịch sau khi trộn gồm :
\(n_{H^+}=0,01+0,012.2=0,034\left(mol\right)\)
=> \(\left[H^+\right]=\dfrac{0,034}{0,5}=0,068M\)
\(n_{NO_3^-}=0,01\left(mol\right)\)
=>\(\left[NO_3^-\right]=\dfrac{0,01}{0,5}=0,02M\)
\(n_{SO_4^{2-}}=0,012\left(mol\right)\)
=> \(\left[SO_4^{2-}\right]=\dfrac{0,012}{0,5}=0,024M\)


\(C\%_{sau}=0,2=\dfrac{100.1,84.0,98}{100.1,84+V_{H_2O}}\\ V_{H_2O}=717,6mL\)

\(19.\\ a)n_{Mg}=\dfrac{2,4}{24}=0,1mol\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ n_{H_2}=n_{H_2SO_4}=n_{Mg}=0,1mol\\ V_{H_2}=0,1.22,4=2,24l\\ b)m_{ddH_2SO_4}=\dfrac{0,1.98}{10}\cdot100=98g\)

Câu 3 :
2NaCl + H2SO4 -------> Na2SO4 + 2HCl1___________________________1
vậy %HCl = 36.5/(36.5 + 146 ) = 20 %
Câu 1 : 9,71
Câu 2 :
gọi a,b lần lượt là số mol của H2SO4 ban đầu và SO3 thêm vàokhối lượng dd H2SO4 ban đầu=980a gam
khối lượng SO3 thêm jhjjh
=>980a+80b=100
pt: SO3+H2O--->H2SO4
mol b--------------->b
tong sồ mol H2SO4 sau phản ứng là a+b=20/98 giải hệ được
b=1/9 => khối lượng SO3 là 80/9 gam

\(V_{ddH_2SO_4\left(98\%\right)}=a\left(ml\right);V_{H_2O}=b\left(ml\right)\\ \Rightarrow a+b=100\left(1\right)\\ Mặt.khác:\dfrac{0,98a}{a+b}.100\%=20\%\\ \Leftrightarrow0,98a=0,2a+0,2b\\ \Leftrightarrow0,78a-0,2b=0\left(2\right)\\ \left(1\right),\left(2\right)\Rightarrow a\approx16,95\left(ml\right);b\approx83,05\left(ml\right)\)
Vậy cần có khoảng 83,05 ml nước và khoảng 16,95 ml dung dịch axit sunfuric 98%