Hòa tan 6,9 gam Na vào H2O được dung dịch X. Thể tích dung dịch HCl 1M cần dùng để phản ứng hết với dung dịch X là ?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

14 tháng 3 2019
Đáp án D
nH2 = 3,36 : 22,4 = 0,15 (mol)
=> nOH- = 2nH2 = 0,3 (mol)
H+ + OH- → H2O
nH + = nOH - = 0,3 (mol)
Mặt khác: nH+ = nHCl + 2nH2SO4 = V + 2V = 3V (mol)
=> 3V = 0,3 => V =0,1 (lít) = 100 (ml)

28 tháng 12 2019
Giải thích:
nH2 = 3,36 : 22,4 = 0,15 (mol)
=> nOH- = 2nH2 = 0,3 (mol)
H+ + OH- → H2O
nH + = nOH - = 0,3 (mol)
Mặt khác: nH+ = nHCl + 2nH2SO4 = V + 2V = 3V (mol)
=> 3V = 0,3 => V =0,1 (lít) = 100 (ml)
Đáp án D

14 tháng 3 2017
Giải thích: Đáp án D
Glutamic: 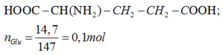
Ta có ∶ Glu + (HCl,H2SO4) ⟶ Muối
Bảo toàn khối lượng ta có :
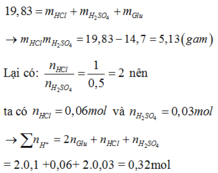
Suy ra số mol OH− cần để phản ứng với số chất tan trong dung dịch X cũng là số mol OH−phản ứng với tổng số mol H+
![]()
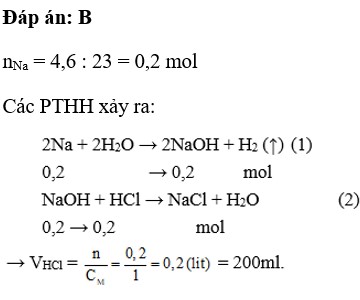
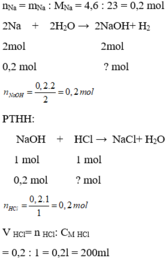
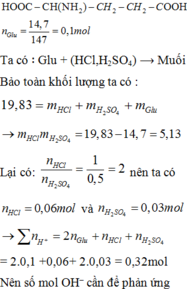

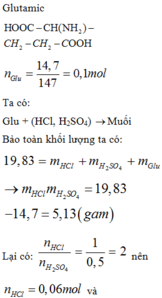

\(n_{Na}=\dfrac{6,9}{23}=0,3\left(mol\right)\)
PTHH: 2Na + 2H2O ---> 2NaOH + H2
0,3---------------->0,3
NaOH + HCl ---> NaCl + H2O
0,3---->0,3
=> \(V_{ddHCl}=\dfrac{0,3}{1}=0,3\left(l\right)=300\left(ml\right)\)