có 6g hỗn hợp gồm Mg và MgO tác dụng với HCl 7,3% thì thu được 2,24 lít khí ở đktc
a,viết phương trình phản úng xảy ra
b,tính khối lượng và thành phần phần trăm các chất trong hỗn hợp đầu ?
c, tính khối lượng dung dịch HCl cần dùng
( Biết :Mg=24,O=16,H=1,Cl=35,5,Cu=64)


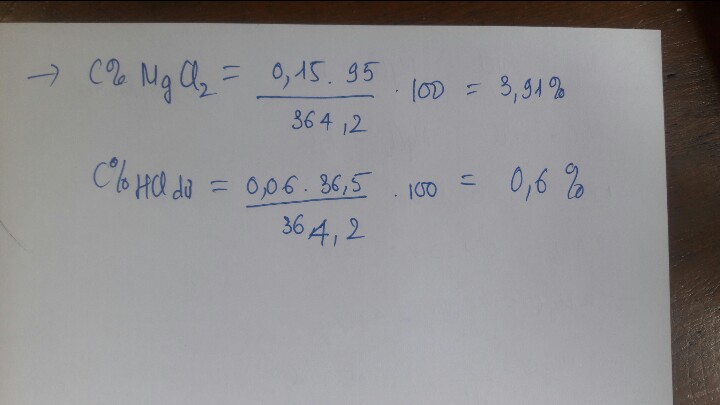
a, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
b, Ta có: \(n_{H_2}=0,1\left(mol\right)\)
Theo PT: \(n_{Mg}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,1.24=2,4\left(g\right)\Rightarrow\%m_{Mg}=\dfrac{2,4}{6}.100\%=40\%\)
⇒ mMgO = 6 - 2,4 = 3,6 (g) \(\Rightarrow\%m_{MgO}=\dfrac{3,6}{6}.100\%=60\%\)
c, Ta có: \(n_{MgO}=\dfrac{3,6}{40}=0,09\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Mg}+2n_{MgO}=0,38\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{0,38.36,5}{7,3\%}=190\left(g\right)\)
cảm ơn nhiều